Mempelajari konsep kalor di kelas 11 bisa jadi seru, lho! Bayangkan, kamu bisa memahami bagaimana panas berpindah dari satu benda ke benda lain, atau bagaimana es batu bisa mencair. Nah, untuk menguji pemahamanmu, yuk kita bahas contoh soal kalor kelas 11 yang menarik dan menantang!
Contoh soal ini akan mengantarkanmu pada berbagai konsep penting, seperti pengertian kalor, perpindahan kalor, kalor jenis, kalor lebur, kalor uap, dan aplikasi kalor dalam kehidupan sehari-hari. Dengan memahami konsep-konsep ini, kamu akan semakin mahir dalam menyelesaikan soal-soal kalor dan mengaplikasikannya dalam berbagai situasi.
Konsep Kalor
Kalor adalah energi panas yang berpindah dari benda yang bersuhu lebih tinggi ke benda yang bersuhu lebih rendah. Dalam kehidupan sehari-hari, kita sering merasakan efek dari perpindahan kalor, misalnya ketika kita memegang secangkir kopi panas, tangan kita akan terasa hangat karena kalor berpindah dari kopi ke tangan kita. Atau saat kita menjemur pakaian di bawah sinar matahari, pakaian tersebut akan terasa panas karena menyerap kalor dari sinar matahari.
Perbedaan Kalor dan Suhu
Kalor dan suhu seringkali disamakan, padahal keduanya memiliki perbedaan yang mendasar. Suhu adalah ukuran derajat panas atau dinginnya suatu benda. Sedangkan kalor adalah energi panas yang berpindah.
Sebagai contoh, bayangkan dua benda dengan ukuran yang sama, satu terbuat dari logam dan satunya lagi terbuat dari kayu. Kedua benda tersebut dipanaskan hingga mencapai suhu yang sama. Meskipun keduanya memiliki suhu yang sama, benda logam akan terasa lebih panas karena logam memiliki kapasitas kalor yang lebih kecil daripada kayu. Artinya, logam membutuhkan kalor yang lebih sedikit untuk meningkatkan suhunya dibandingkan kayu.
Jenis-jenis Kalor
Kalor dapat dibedakan menjadi beberapa jenis berdasarkan cara perpindahannya, yaitu:
- Konduksi: Perpindahan kalor melalui zat perantara tanpa disertai perpindahan zat perantaranya. Contohnya adalah ketika kita memegang ujung logam yang dipanaskan, panas akan merambat ke tangan kita melalui logam tersebut.
- Konveksi: Perpindahan kalor melalui pergerakan zat perantara. Contohnya adalah ketika kita merebus air, air yang berada di dasar panci akan menerima kalor dari api dan menjadi lebih panas. Air panas ini kemudian akan bergerak ke atas dan digantikan oleh air dingin yang berada di atasnya. Proses ini terus berulang sehingga seluruh air dalam panci menjadi panas.
- Radiasi: Perpindahan kalor melalui gelombang elektromagnetik. Contohnya adalah ketika kita merasakan panas dari matahari, panas tersebut berpindah ke bumi melalui radiasi elektromagnetik.
Perpindahan Kalor
Kalor merupakan bentuk energi yang berpindah dari benda bersuhu tinggi ke benda bersuhu rendah. Perpindahan kalor ini dapat terjadi melalui beberapa cara, yaitu konduksi, konveksi, dan radiasi. Masing-masing cara perpindahan kalor memiliki mekanisme dan karakteristik yang berbeda.
Konduksi
Konduksi adalah perpindahan kalor melalui perantara zat tanpa disertai perpindahan zat perantaranya. Perhatikan contoh berikut:
- Saat kamu memegang sendok logam yang dipanaskan, panas dari ujung sendok yang dipanaskan akan merambat ke ujung sendok yang kamu pegang. Panas merambat melalui logam tanpa disertai perpindahan logam itu sendiri.
- Ketika kamu menempelkan tanganmu ke permukaan besi yang panas, panas dari besi akan merambat ke tanganmu melalui kontak langsung. Panas merambat melalui besi tanpa disertai perpindahan besi itu sendiri.
Kecepatan perpindahan kalor secara konduksi dipengaruhi oleh beberapa faktor, antara lain:
- Jenis zat: Zat yang memiliki konduktivitas termal tinggi, seperti logam, akan lebih cepat menghantarkan kalor dibandingkan zat yang memiliki konduktivitas termal rendah, seperti kayu atau plastik.
- Luas permukaan: Semakin luas permukaan benda, semakin cepat kalor akan merambat.
- Perbedaan suhu: Semakin besar perbedaan suhu antara dua benda, semakin cepat kalor akan merambat.
- Ketebalan benda: Semakin tebal benda, semakin lambat kalor akan merambat.
Konveksi
Konveksi adalah perpindahan kalor melalui perantara zat yang disertai perpindahan zat perantaranya. Perhatikan contoh berikut:
- Air yang dipanaskan dalam panci akan mendidih. Air yang panas akan naik ke permukaan, sementara air yang dingin akan turun ke dasar panci. Proses ini terjadi karena air yang panas memiliki massa jenis yang lebih rendah daripada air yang dingin, sehingga air yang panas akan naik ke permukaan.
- Angin yang bertiup adalah contoh perpindahan kalor secara konveksi. Udara yang panas akan naik ke atas, sementara udara yang dingin akan turun ke bawah. Proses ini terjadi karena udara yang panas memiliki massa jenis yang lebih rendah daripada udara yang dingin, sehingga udara yang panas akan naik ke atas.
Kecepatan perpindahan kalor secara konveksi dipengaruhi oleh beberapa faktor, antara lain:
- Perbedaan suhu: Semakin besar perbedaan suhu antara dua benda, semakin cepat kalor akan merambat.
- Sifat zat: Zat yang memiliki viskositas rendah, seperti air, akan lebih mudah mengalami konveksi dibandingkan zat yang memiliki viskositas tinggi, seperti minyak.
- Luas permukaan: Semakin luas permukaan benda, semakin cepat kalor akan merambat.
Radiasi
Radiasi adalah perpindahan kalor tanpa melalui perantara zat. Kalor merambat dalam bentuk gelombang elektromagnetik. Perhatikan contoh berikut:
- Panjang gelombang radiasi yang dipancarkan oleh benda tergantung pada suhu benda. Semakin tinggi suhu benda, semakin pendek panjang gelombang radiasi yang dipancarkan. Misalnya, matahari memancarkan radiasi inframerah, yang merupakan gelombang elektromagnetik dengan panjang gelombang yang lebih pendek dibandingkan dengan gelombang radio.
- Saat kamu berdiri di dekat api unggun, kamu akan merasakan panas dari api unggun. Panas ini merambat ke tubuhmu dalam bentuk radiasi inframerah.
Kecepatan perpindahan kalor secara radiasi dipengaruhi oleh beberapa faktor, antara lain:
- Suhu benda: Semakin tinggi suhu benda, semakin cepat kalor akan merambat.
- Luas permukaan: Semakin luas permukaan benda, semakin cepat kalor akan merambat.
- Warna benda: Benda yang berwarna gelap akan menyerap lebih banyak kalor dibandingkan benda yang berwarna terang.
Kalor Lebur dan Kalor Uap
Dalam mempelajari perubahan wujud zat, kita mengenal istilah kalor lebur dan kalor uap. Kedua istilah ini menggambarkan energi yang dibutuhkan untuk mengubah wujud zat dari padat ke cair dan dari cair ke gas, atau sebaliknya. Dalam artikel ini, kita akan membahas lebih lanjut mengenai kalor lebur dan kalor uap, termasuk proses perubahan wujud zat yang melibatkan keduanya.
Pengertian Kalor Lebur dan Kalor Uap
Kalor lebur adalah jumlah kalor yang diperlukan untuk mengubah 1 gram zat padat menjadi zat cair pada titik leburnya tanpa perubahan suhu. Kalor lebur dilambangkan dengan L, dan satuannya adalah Joule per gram (J/g) atau kalori per gram (kal/g). Sebagai contoh, kalor lebur es adalah 334 J/g, yang artinya diperlukan 334 Joule energi untuk mengubah 1 gram es menjadi air pada suhu 0 derajat Celcius.
Kalor uap, di sisi lain, adalah jumlah kalor yang diperlukan untuk mengubah 1 gram zat cair menjadi zat gas pada titik didihnya tanpa perubahan suhu. Kalor uap dilambangkan dengan U, dan satuannya juga Joule per gram (J/g) atau kalori per gram (kal/g). Sebagai contoh, kalor uap air adalah 2260 J/g, yang artinya diperlukan 2260 Joule energi untuk mengubah 1 gram air menjadi uap air pada suhu 100 derajat Celcius.
Proses Perubahan Wujud Zat
Proses perubahan wujud zat yang melibatkan kalor lebur dan kalor uap dapat dijelaskan sebagai berikut:
- Melebur: Proses perubahan wujud zat padat menjadi zat cair. Kalor lebur diperlukan untuk mengatasi gaya tarik-menarik antar molekul dalam zat padat sehingga molekul-molekul tersebut dapat bergerak bebas dan membentuk zat cair. Contohnya, ketika es dipanaskan, kalor lebur akan digunakan untuk mengubah es menjadi air.
- Membeku: Proses perubahan wujud zat cair menjadi zat padat. Proses ini adalah kebalikan dari melebur, di mana kalor lebur dilepaskan saat molekul-molekul dalam zat cair kehilangan energi dan membentuk ikatan yang lebih kuat, sehingga membentuk zat padat.
- Menguap: Proses perubahan wujud zat cair menjadi zat gas. Kalor uap diperlukan untuk mengatasi gaya tarik-menarik antar molekul dalam zat cair sehingga molekul-molekul tersebut dapat bergerak bebas dan membentuk zat gas. Contohnya, ketika air dipanaskan, kalor uap akan digunakan untuk mengubah air menjadi uap air.
- Mengembun: Proses perubahan wujud zat gas menjadi zat cair. Proses ini adalah kebalikan dari menguap, di mana kalor uap dilepaskan saat molekul-molekul dalam zat gas kehilangan energi dan membentuk ikatan yang lebih kuat, sehingga membentuk zat cair.
- Mensublimasi: Proses perubahan wujud zat padat langsung menjadi zat gas. Proses ini tidak melibatkan fase cair, dan kalor sublimasi diperlukan untuk mengatasi gaya tarik-menarik antar molekul dalam zat padat sehingga molekul-molekul tersebut dapat bergerak bebas dan membentuk zat gas. Contohnya, kapur barus yang lama kelamaan akan habis karena menyublim menjadi gas.
- Menyublim: Proses perubahan wujud zat gas langsung menjadi zat padat. Proses ini adalah kebalikan dari menyublimasi, di mana kalor sublimasi dilepaskan saat molekul-molekul dalam zat gas kehilangan energi dan membentuk ikatan yang lebih kuat, sehingga membentuk zat padat.
Diagram Perubahan Wujud Zat
Berikut adalah diagram yang menunjukkan perubahan wujud zat dan peranan kalor lebur dan kalor uap:
| Padat | Cair | Gas | |
| Melebur | Kalor Lebur | ||
| Membeku | Kalor Lebur | ||
| Menguap | Kalor Uap | ||
| Mengembun | Kalor Uap | ||
| Mensublimasi | Kalor Sublimasi | ||
| Menyublim | Kalor Sublimasi |
Diagram ini menunjukkan bahwa kalor lebur diperlukan untuk mengubah zat padat menjadi zat cair, dan kalor uap diperlukan untuk mengubah zat cair menjadi zat gas. Kalor lebur dan kalor uap juga diperlukan untuk proses kebalikannya, yaitu membeku dan mengembun. Selain itu, kalor sublimasi diperlukan untuk proses perubahan wujud zat padat langsung menjadi gas, dan sebaliknya.
Kalorimeter
Kalorimeter adalah alat yang digunakan untuk mengukur jumlah kalor yang terlibat dalam suatu reaksi kimia atau perubahan fisik. Alat ini bekerja berdasarkan prinsip kekekalan energi, di mana energi tidak dapat diciptakan maupun dimusnahkan, hanya dapat diubah bentuknya. Kalorimeter merupakan alat yang penting dalam berbagai bidang, seperti kimia, fisika, dan biologi.
Fungsi Kalorimeter
Kalorimeter memiliki fungsi utama untuk mengukur perubahan kalor yang terjadi dalam suatu sistem. Perubahan kalor ini dapat berupa kalor yang diserap atau dilepaskan oleh sistem.
Prinsip Kerja Kalorimeter
Prinsip kerja kalorimeter didasarkan pada konsep kekekalan energi. Kalor yang dilepaskan oleh sistem akan diserap oleh kalorimeter dan lingkungan sekitarnya. Dengan mengukur perubahan suhu kalorimeter dan lingkungannya, kita dapat menghitung jumlah kalor yang dilepaskan oleh sistem.
Contoh Soal Perhitungan Kalor Menggunakan Kalorimeter
Sebuah kalorimeter berisi 100 gram air pada suhu 25 derajat Celcius. Kemudian, 50 gram logam panas dengan suhu 100 derajat Celcius dimasukkan ke dalam kalorimeter. Setelah mencapai kesetimbangan termal, suhu air dan logam menjadi 28 derajat Celcius. Jika kalor jenis air adalah 4,18 J/g°C dan kalor jenis logam adalah 0,385 J/g°C, tentukan kalor yang dilepaskan oleh logam.
Berikut langkah-langkah untuk menyelesaikan soal tersebut:
- Hitung kalor yang diserap oleh air:
- Hitung kalor yang dilepaskan oleh logam:
Qair = mair x cair x ΔTair
Qair = 100 g x 4,18 J/g°C x (28°C – 25°C)
Qair = 1254 J
Qlogam = mlogam x clogam x ΔTlogam
Qlogam = 50 g x 0,385 J/g°C x (100°C – 28°C)
Qlogam = 1386 J
Jadi, kalor yang dilepaskan oleh logam adalah 1386 J.
Penerapan Kalor dalam Kehidupan Sehari-hari
Kalor merupakan bentuk energi yang berpindah dari benda bersuhu tinggi ke benda bersuhu rendah. Konsep kalor memiliki peran penting dalam berbagai aspek kehidupan sehari-hari, mulai dari memasak hingga teknologi canggih. Dalam artikel ini, kita akan menjelajahi beberapa contoh penerapan konsep kalor dalam kehidupan sehari-hari, alat yang memanfaatkannya, serta dampak positif dan negatifnya.
Contoh Penerapan Kalor dalam Kehidupan Sehari-hari
Konsep kalor banyak dijumpai dalam kehidupan sehari-hari. Berikut adalah beberapa contohnya:
- Memasak: Proses memasak makanan melibatkan perpindahan kalor dari sumber panas (kompor, oven) ke bahan makanan. Kalor menyebabkan perubahan suhu dan struktur bahan makanan, sehingga menjadi matang dan siap dikonsumsi.
- Menyetrika: Menyetrika pakaian memanfaatkan kalor untuk menghaluskan lipatan dan kerutan. Kalor dari setrika akan meratakan serat kain dan membuatnya lebih rapi.
- Mandi Air Hangat: Mandi air hangat memberikan sensasi relaksasi dan menghangatkan tubuh. Kalor dari air hangat akan diserap oleh tubuh dan meningkatkan suhu tubuh.
- Pengering Rambut: Pengering rambut memanfaatkan kalor untuk mengeringkan rambut basah. Kalor dari pengering rambut akan menguapkan air pada rambut dan membuatnya kering.
Alat yang Memanfaatkan Konsep Kalor
Banyak alat yang memanfaatkan konsep kalor dalam kerjanya. Berikut adalah beberapa contohnya:
- Mesin Uap: Mesin uap memanfaatkan kalor untuk menghasilkan tenaga mekanik. Kalor dari pembakaran bahan bakar akan mengubah air menjadi uap, yang kemudian digunakan untuk menggerakkan turbin.
- Pembangkit Listrik Tenaga Uap: Pembangkit listrik tenaga uap memanfaatkan kalor untuk menghasilkan energi listrik. Kalor dari pembakaran bahan bakar akan menghasilkan uap yang menggerakkan turbin, yang kemudian menghasilkan energi listrik.
- Kulkas: Kulkas memanfaatkan konsep kalor untuk mendinginkan makanan. Kalor dari makanan akan diserap oleh fluida pendingin, yang kemudian dialirkan ke luar kulkas.
- AC: AC memanfaatkan konsep kalor untuk mendinginkan ruangan. Kalor dari ruangan akan diserap oleh fluida pendingin, yang kemudian dialirkan ke luar ruangan.
Dampak Positif dan Negatif Penggunaan Kalor, Contoh soal kalor kelas 11
Penggunaan kalor dalam kehidupan sehari-hari memiliki dampak positif dan negatif. Berikut adalah beberapa contohnya:
- Dampak Positif:
- Memudahkan proses memasak dan pengolahan makanan.
- Meningkatkan kenyamanan dan kesehatan, seperti mandi air hangat dan penggunaan AC.
- Membantu dalam proses produksi berbagai barang dan jasa, seperti industri manufaktur dan pembangkit listrik.
- Dampak Negatif:
- Pencemaran lingkungan, seperti emisi gas rumah kaca dari pembangkit listrik tenaga uap.
- Bahaya kebakaran, jika penggunaan kalor tidak diawasi dengan baik.
- Kerusakan alat, jika penggunaan kalor tidak sesuai dengan petunjuk.
Soal Latihan
Setelah mempelajari materi tentang kalor, saatnya untuk menguji pemahamanmu dengan mengerjakan soal-soal latihan berikut. Soal-soal ini dirancang dengan tingkat kesulitan sedang, meliputi berbagai konsep penting dalam kalor. Selamat mencoba!
Soal Pilihan Ganda
Pilihlah satu jawaban yang paling tepat untuk setiap soal berikut.
Contoh soal kalor kelas 11 biasanya membahas tentang perpindahan energi panas, seperti menghitung kalor jenis atau perubahan suhu suatu benda. Nah, untuk memahami konsep kalor, kamu juga perlu memahami konsep barisan geometri. Misalnya, ketika menghitung jumlah kalor yang dibutuhkan untuk menaikkan suhu suatu benda, kamu bisa menggunakan rumus barisan geometri.
Kamu bisa mempelajari lebih lanjut tentang contoh soal barisan geometri kelas 11 di sini: contoh soal barisan geometri kelas 11. Dengan memahami konsep barisan geometri, kamu akan lebih mudah dalam menyelesaikan contoh soal kalor kelas 11!
- Suatu benda bermassa 2 kg dipanaskan dari suhu 20°C menjadi 80°C. Jika kalor jenis benda tersebut 400 J/kg°C, maka kalor yang diperlukan untuk memanaskan benda tersebut adalah …
- Sebuah bejana berisi 500 gram air bersuhu 20°C dicampur dengan 200 gram air bersuhu 80°C. Jika kalor jenis air 4200 J/kg°C, maka suhu campuran air tersebut adalah …
- Sebuah logam bermassa 100 gram dipanaskan dari suhu 20°C menjadi 60°C. Jika kalor yang diperlukan untuk memanaskan logam tersebut 2000 J, maka kalor jenis logam tersebut adalah …
- Sebuah benda bermassa 500 gram dengan kalor jenis 800 J/kg°C dipanaskan dari suhu 25°C menjadi 75°C. Kalor yang diserap benda tersebut adalah …
- Sebuah bejana berisi 200 gram air bersuhu 30°C dicampur dengan 100 gram air bersuhu 70°C. Jika kalor jenis air 4200 J/kg°C, maka suhu campuran air tersebut adalah …
Soal Uraian
Jawablah pertanyaan berikut dengan jelas dan lengkap.
- Jelaskan perbedaan antara kalor jenis dan kapasitas kalor! Berikan contoh masing-masing.
- Sebuah logam bermassa 200 gram dipanaskan dari suhu 20°C menjadi 80°C. Jika kalor yang diserap logam tersebut 4000 J, tentukan kalor jenis logam tersebut!
- Sebuah bejana berisi 500 gram air bersuhu 25°C dicampur dengan 200 gram air bersuhu 60°C. Jika kalor jenis air 4200 J/kg°C, tentukan suhu akhir campuran air tersebut!
- Jelaskan prinsip kerja kalorimeter! Berikan contoh penggunaan kalorimeter dalam kehidupan sehari-hari!
- Sebuah benda bermassa 1 kg dengan kalor jenis 400 J/kg°C dipanaskan dari suhu 20°C menjadi 60°C. Hitunglah kalor yang diserap benda tersebut!
Kunci Jawaban dan Pembahasan
Berikut adalah kunci jawaban dan pembahasan untuk soal-soal latihan di atas.
Soal Pilihan Ganda
- Jawaban: 48.000 J
Pembahasan:
Kalor yang diperlukan untuk memanaskan benda dapat dihitung dengan rumus:
Q = m x c x ΔT
dengan:
Q = kalor (J)
m = massa (kg)
c = kalor jenis (J/kg°C)
ΔT = perubahan suhu (°C)
Maka, kalor yang diperlukan untuk memanaskan benda tersebut adalah:
Q = 2 kg x 400 J/kg°C x (80°C – 20°C) = 48.000 J - Jawaban: 32°C
Pembahasan:
Suhu campuran air dapat dihitung dengan rumus:
T = (m1 x T1 + m2 x T2) / (m1 + m2)
dengan:
T = suhu campuran (°C)
m1 = massa air 1 (kg)
T1 = suhu air 1 (°C)
m2 = massa air 2 (kg)
T2 = suhu air 2 (°C)
Maka, suhu campuran air tersebut adalah:
T = (0,5 kg x 20°C + 0,2 kg x 80°C) / (0,5 kg + 0,2 kg) = 32°C - Jawaban: 400 J/kg°C
Pembahasan:
Kalor jenis logam dapat dihitung dengan rumus:
c = Q / (m x ΔT)
dengan:
c = kalor jenis (J/kg°C)
Q = kalor (J)
m = massa (kg)
ΔT = perubahan suhu (°C)
Maka, kalor jenis logam tersebut adalah:
c = 2000 J / (0,1 kg x (60°C – 20°C)) = 400 J/kg°C - Jawaban: 20.000 J
Pembahasan:
Kalor yang diserap benda dapat dihitung dengan rumus:
Q = m x c x ΔT
dengan:
Q = kalor (J)
m = massa (kg)
c = kalor jenis (J/kg°C)
ΔT = perubahan suhu (°C)
Maka, kalor yang diserap benda tersebut adalah:
Q = 0,5 kg x 800 J/kg°C x (75°C – 25°C) = 20.000 J - Jawaban: 40°C
Pembahasan:
Suhu campuran air dapat dihitung dengan rumus:
T = (m1 x T1 + m2 x T2) / (m1 + m2)
dengan:
T = suhu campuran (°C)
m1 = massa air 1 (kg)
T1 = suhu air 1 (°C)
m2 = massa air 2 (kg)
T2 = suhu air 2 (°C)
Maka, suhu campuran air tersebut adalah:
T = (0,2 kg x 30°C + 0,1 kg x 70°C) / (0,2 kg + 0,1 kg) = 40°C
Soal Uraian
- Pembahasan:
Kalor jenis adalah jumlah kalor yang diperlukan untuk menaikkan suhu 1 kg zat sebesar 1°C. Sedangkan kapasitas kalor adalah jumlah kalor yang diperlukan untuk menaikkan suhu suatu benda sebesar 1°C.
Contoh kalor jenis: Kalor jenis air adalah 4200 J/kg°C, artinya diperlukan 4200 J kalor untuk menaikkan suhu 1 kg air sebesar 1°C.
Contoh kapasitas kalor: Kapasitas kalor sebuah panci adalah 200 J/°C, artinya diperlukan 200 J kalor untuk menaikkan suhu panci tersebut sebesar 1°C. - Pembahasan:
Kalor jenis logam dapat dihitung dengan rumus:
c = Q / (m x ΔT)
dengan:
c = kalor jenis (J/kg°C)
Q = kalor (J)
m = massa (kg)
ΔT = perubahan suhu (°C)
Maka, kalor jenis logam tersebut adalah:
c = 4000 J / (0,2 kg x (80°C – 20°C)) = 333,33 J/kg°C - Pembahasan:
Suhu akhir campuran air dapat dihitung dengan rumus:
T = (m1 x T1 + m2 x T2) / (m1 + m2)
dengan:
T = suhu campuran (°C)
m1 = massa air 1 (kg)
T1 = suhu air 1 (°C)
m2 = massa air 2 (kg)
T2 = suhu air 2 (°C)
Maka, suhu akhir campuran air tersebut adalah:
T = (0,5 kg x 25°C + 0,2 kg x 60°C) / (0,5 kg + 0,2 kg) = 35°C - Pembahasan:
Kalorimeter adalah alat yang digunakan untuk mengukur kalor yang dilepaskan atau diserap dalam suatu reaksi kimia atau proses fisika. Prinsip kerja kalorimeter adalah berdasarkan asas Black, yaitu kalor yang dilepaskan oleh benda yang lebih panas sama dengan kalor yang diserap oleh benda yang lebih dingin. Kalorimeter biasanya terdiri dari wadah berisolasi yang berisi air, termometer untuk mengukur suhu air, dan pengaduk untuk mencampur air.
Contoh penggunaan kalorimeter dalam kehidupan sehari-hari: Kalorimeter dapat digunakan untuk menentukan kalor pembakaran bahan bakar, seperti kayu atau batu bara. Kalorimeter juga dapat digunakan untuk menentukan kalor jenis suatu zat. - Pembahasan:
Kalor yang diserap benda dapat dihitung dengan rumus:
Q = m x c x ΔT
dengan:
Q = kalor (J)
m = massa (kg)
c = kalor jenis (J/kg°C)
ΔT = perubahan suhu (°C)
Maka, kalor yang diserap benda tersebut adalah:
Q = 1 kg x 400 J/kg°C x (60°C – 20°C) = 16.000 J
Penjelasan Konsep Kalor
Kalor adalah bentuk energi yang berpindah dari benda yang bersuhu lebih tinggi ke benda yang bersuhu lebih rendah. Kalor dapat berpindah melalui tiga cara, yaitu konduksi, konveksi, dan radiasi. Konduksi adalah perpindahan kalor melalui zat perantara tanpa disertai perpindahan partikel zat perantaranya. Contohnya, ketika kamu memegang sendok logam yang dipanaskan di atas api, kalor akan berpindah dari ujung sendok yang panas ke ujung sendok yang kamu pegang melalui konduksi. Konveksi adalah perpindahan kalor melalui pergerakan zat perantara. Contohnya, ketika air dipanaskan, air di bagian bawah akan memuai dan menjadi lebih ringan, sehingga naik ke permukaan. Air yang lebih dingin di permukaan akan turun ke bagian bawah untuk dipanaskan, dan proses ini akan berulang. Radiasi adalah perpindahan kalor tanpa memerlukan zat perantara. Contohnya, panas matahari yang sampai ke bumi adalah contoh perpindahan kalor melalui radiasi.
Hubungan Kalor, Suhu, dan Perubahan Wujud Zat
Kalor, suhu, dan perubahan wujud zat memiliki hubungan yang erat. Kalor adalah energi yang berpindah, sedangkan suhu adalah ukuran energi kinetik rata-rata partikel dalam suatu zat. Ketika suatu zat menyerap kalor, energi kinetik rata-rata partikelnya akan meningkat, sehingga suhunya akan naik. Sebaliknya, ketika suatu zat melepaskan kalor, energi kinetik rata-rata partikelnya akan menurun, sehingga suhunya akan turun.
Perubahan wujud zat terjadi ketika kalor yang diserap atau dilepas oleh zat cukup besar untuk mengubah energi kinetik rata-rata partikelnya. Ketika suatu zat menyerap kalor, energi kinetik rata-rata partikelnya akan meningkat, sehingga jarak antar partikel akan semakin besar. Jika kalor yang diserap cukup besar, zat tersebut akan berubah wujud dari padat menjadi cair (mencair) atau dari cair menjadi gas (menguap). Sebaliknya, ketika suatu zat melepaskan kalor, energi kinetik rata-rata partikelnya akan menurun, sehingga jarak antar partikel akan semakin kecil. Jika kalor yang dilepas cukup besar, zat tersebut akan berubah wujud dari gas menjadi cair (mengembun) atau dari cair menjadi padat (membeku).
Proses Perpindahan Kalor
Proses perpindahan kalor dapat diilustrasikan dengan diagram berikut:
Gambar 1: Proses Perpindahan Kalor
Gambar ini menunjukkan tiga cara perpindahan kalor: konduksi, konveksi, dan radiasi. Konduksi terjadi ketika kalor berpindah melalui zat perantara tanpa disertai perpindahan partikel zat perantaranya. Konveksi terjadi ketika kalor berpindah melalui pergerakan zat perantara. Radiasi terjadi ketika kalor berpindah tanpa memerlukan zat perantara.
Perpindahan kalor memiliki peranan penting dalam kehidupan sehari-hari. Contohnya, ketika kita memasak air di atas kompor, kalor dari api kompor akan berpindah ke panci melalui konduksi. Kemudian, kalor akan berpindah ke air di dalam panci melalui konveksi. Ketika kita menjemur pakaian di bawah sinar matahari, kalor dari matahari akan berpindah ke pakaian melalui radiasi. Selain itu, perpindahan kalor juga berperan dalam berbagai proses alam, seperti siklus air, angin, dan cuaca.
Perhitungan Kalor
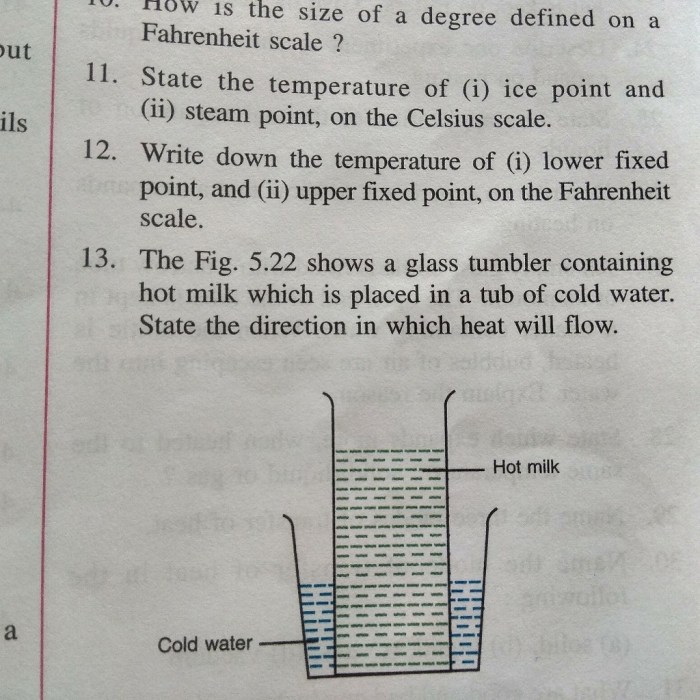
Kalor merupakan bentuk energi yang berpindah dari benda yang bersuhu lebih tinggi ke benda yang bersuhu lebih rendah. Perhitungan kalor melibatkan beberapa faktor, seperti massa benda, jenis benda, dan perubahan suhu.
Rumus Perhitungan Kalor
Rumus perhitungan kalor dapat dibedakan menjadi beberapa jenis, tergantung pada perubahan keadaan benda. Berikut adalah beberapa rumus yang umum digunakan:
- Kalor untuk menaikkan suhu: Q = m.c.ΔT, dengan:
- Q adalah kalor (Joule)
- m adalah massa benda (kg)
- c adalah kalor jenis benda (J/kg°C)
- ΔT adalah perubahan suhu (°C)
- Kalor untuk melebur: Q = m.L, dengan:
- Q adalah kalor lebur (Joule)
- m adalah massa benda (kg)
- L adalah kalor lebur benda (J/kg)
- Kalor untuk menguapkan: Q = m.U, dengan:
- Q adalah kalor uap (Joule)
- m adalah massa benda (kg)
- U adalah kalor uap benda (J/kg)
Contoh Soal Perhitungan Kalor
Berikut adalah contoh soal perhitungan kalor dan langkah-langkah penyelesaiannya:
Sebuah balok besi dengan massa 2 kg dipanaskan dari suhu 20°C hingga 80°C. Jika kalor jenis besi adalah 450 J/kg°C, tentukan kalor yang dibutuhkan untuk memanaskan balok besi tersebut!
Penyelesaian:
- Diketahui: m = 2 kg, c = 450 J/kg°C, ΔT = 80°C – 20°C = 60°C
- Ditanya: Q = …?
- Jawab: Q = m.c.ΔT = 2 kg x 450 J/kg°C x 60°C = 54.000 Joule
Menentukan Nilai Kalor Jenis, Kalor Lebur, dan Kalor Uap
Nilai kalor jenis, kalor lebur, dan kalor uap dapat ditentukan melalui tabel atau eksperimen.
- Kalor jenis adalah jumlah kalor yang dibutuhkan untuk menaikkan suhu 1 kg suatu zat sebesar 1°C. Nilai kalor jenis berbeda-beda untuk setiap zat.
- Kalor lebur adalah jumlah kalor yang dibutuhkan untuk melebur 1 kg zat padat menjadi zat cair pada titik leburnya. Nilai kalor lebur juga berbeda-beda untuk setiap zat.
- Kalor uap adalah jumlah kalor yang dibutuhkan untuk menguapkan 1 kg zat cair menjadi zat uap pada titik didihnya. Nilai kalor uap juga berbeda-beda untuk setiap zat.
Penerapan Kalor dalam Industri
Kalor, sebagai bentuk energi yang berpindah akibat perbedaan suhu, memegang peranan penting dalam berbagai proses industri. Penerapan konsep kalor dalam industri memiliki dampak yang luas, baik positif maupun negatif.
Contoh Penerapan Konsep Kalor dalam Industri
Konsep kalor diterapkan dalam berbagai proses industri, baik untuk menghasilkan produk, meningkatkan efisiensi, maupun meminimalkan dampak lingkungan. Berikut beberapa contohnya:
- Pembangkitan Listrik: Pembangkit listrik tenaga uap memanfaatkan kalor yang dihasilkan dari pembakaran bahan bakar fosil untuk menguapkan air, menghasilkan uap bertekanan tinggi yang memutar turbin dan menghasilkan energi listrik.
- Industri Pengolahan Makanan: Proses pemanasan dan pengeringan makanan memanfaatkan kalor untuk membunuh bakteri, mengawetkan makanan, dan mengubah tekstur makanan. Contohnya, proses pasteurisasi susu, pengeringan buah, dan pemanggangan roti.
- Industri Kimia: Kalor digunakan dalam berbagai reaksi kimia, seperti sintesis bahan kimia, pemisahan campuran, dan pengolahan logam. Contohnya, proses produksi pupuk, plastik, dan logam.
- Industri Metalurgi: Kalor digunakan untuk melebur logam, membentuk logam, dan memperkuat logam. Contohnya, proses peleburan besi, pembuatan baja, dan perlakuan panas logam.
Proses Industri yang Memanfaatkan Konsep Kalor
Berikut beberapa contoh proses industri yang memanfaatkan konsep kalor:
- Pembuatan Kaca: Pembuatan kaca melibatkan pemanasan pasir silika hingga meleleh, kemudian didinginkan secara perlahan untuk menghasilkan kaca yang kuat dan tahan lama.
- Pembuatan Semen: Proses pembuatan semen melibatkan pemanasan campuran bahan baku, seperti batu kapur, tanah liat, dan pasir, hingga mencapai suhu tinggi, sehingga terjadi reaksi kimia yang menghasilkan semen.
- Pengolahan Minyak Bumi: Proses pengolahan minyak bumi melibatkan pemanasan minyak bumi untuk memisahkan berbagai komponen, seperti bensin, solar, dan minyak tanah.
- Pembuatan Keramik: Proses pembuatan keramik melibatkan pemanasan tanah liat hingga mencapai suhu tinggi, sehingga terjadi perubahan struktur dan sifat tanah liat, menghasilkan keramik yang keras dan tahan lama.
Dampak Positif dan Negatif Penggunaan Kalor dalam Industri
Penggunaan kalor dalam industri memiliki dampak positif dan negatif. Berikut beberapa contohnya:
- Dampak Positif:
- Meningkatkan efisiensi proses produksi.
- Memungkinkan pembuatan produk baru dengan sifat yang lebih baik.
- Mempermudah proses pengolahan bahan baku.
- Dampak Negatif:
- Emisi gas rumah kaca, seperti CO2, yang dapat menyebabkan pemanasan global.
- Polusi udara dan air akibat pembuangan limbah industri.
- Bahaya kebakaran dan ledakan akibat penggunaan bahan bakar yang mudah terbakar.
Penutupan: Contoh Soal Kalor Kelas 11
Melalui contoh soal kalor kelas 11, kita telah menjelajahi berbagai aspek menarik dari konsep kalor. Mulai dari pemahaman dasar tentang panas dan suhu, hingga penerapannya dalam kehidupan sehari-hari dan industri. Dengan pemahaman yang kuat, kamu dapat menghadapi berbagai tantangan dalam mempelajari fisika dan mengaplikasikannya dalam berbagai bidang.