Contoh soal ekuilibrium – Pernahkah Anda bertanya-tanya bagaimana reaksi kimia bisa mencapai titik di mana reaktan dan produk tidak berubah lagi? Itulah inti dari konsep kesetimbangan kimia, sebuah keadaan di mana reaksi maju dan balik berlangsung dengan laju yang sama. Dalam dunia kimia, kesetimbangan adalah konsep penting yang membantu kita memahami bagaimana reaksi berlangsung dan bagaimana faktor-faktor tertentu dapat memengaruhi arah reaksi.
Contoh soal ekuilibrium membantu kita untuk menguji pemahaman tentang konsep ini dan mengaplikasikannya dalam berbagai situasi. Dari memahami bagaimana konsentrasi, suhu, dan tekanan memengaruhi kesetimbangan hingga menghitung konstanta kesetimbangan (Kc dan Kp), contoh soal ini membuka jalan bagi kita untuk menjelajahi dunia kesetimbangan kimia dengan lebih mendalam.
Pengertian Kesetimbangan Kimia
Kesetimbangan kimia merupakan kondisi di mana laju reaksi maju dan laju reaksi balik sama besar. Dalam keadaan ini, konsentrasi reaktan dan produk tidak lagi berubah secara signifikan, meskipun reaksi masih berlangsung. Bayangkan sebuah pesta di mana jumlah orang yang datang dan pergi sama, sehingga jumlah total orang di pesta tetap stabil. Kondisi ini mirip dengan kesetimbangan kimia, di mana jumlah reaktan dan produk tetap konstan meskipun reaksi terus berlangsung.
Contoh Reaksi Kesetimbangan
Berikut adalah contoh reaksi kesetimbangan yang sering kita jumpai dalam kehidupan sehari-hari:
- Pembuatan es batu: Ketika air didinginkan di bawah titik bekunya, terjadi kesetimbangan antara air cair dan es batu. Pada suhu tertentu, laju pembekuan air sama dengan laju pelelehan es, sehingga jumlah air cair dan es batu tetap konstan.
- Pembuatan minuman bersoda: Ketika kita membuka botol minuman bersoda, gas karbon dioksida (CO2) keluar dari larutan. Namun, beberapa CO2 tetap terlarut dalam minuman, membentuk kesetimbangan antara CO2 terlarut dan CO2 gas. Kesetimbangan ini menyebabkan minuman tetap berkarbonasi, meskipun beberapa CO2 telah terlepas.
Perbedaan Reaksi Kesetimbangan dan Reaksi Irreversible
Berikut adalah tabel yang membandingkan ciri-ciri reaksi kesetimbangan dengan reaksi irreversible:
| Ciri | Reaksi Kesetimbangan | Reaksi Irreversible |
|---|---|---|
| Laju reaksi | Laju reaksi maju sama dengan laju reaksi balik | Laju reaksi balik sangat kecil atau tidak terjadi |
| Konsentrasi reaktan dan produk | Tetap konstan setelah mencapai kesetimbangan | Reaktan habis dan produk terbentuk secara sempurna |
| Arah reaksi | Bolak-balik | Hanya satu arah |
| Contoh | Pembuatan es batu, pembuatan minuman bersoda | Pembakaran kayu, reaksi asam kuat dengan basa kuat |
Faktor-faktor yang Mempengaruhi Kesetimbangan
Kesetimbangan kimia merupakan keadaan dinamis di mana laju reaksi maju sama dengan laju reaksi balik. Pada keadaan ini, konsentrasi reaktan dan produk tidak berubah secara makroskopis, meskipun reaksi masih terus berlangsung. Kesetimbangan kimia tidak bersifat statis, melainkan suatu kondisi dinamis yang dapat dipengaruhi oleh beberapa faktor.
Perubahan Konsentrasi Reaktan dan Produk
Perubahan konsentrasi reaktan atau produk dapat menggeser kesetimbangan reaksi. Prinsip Le Chatelier menyatakan bahwa jika suatu sistem kesetimbangan diberi tekanan, sistem tersebut akan bergeser ke arah yang mengurangi tekanan tersebut.
- Penambahan konsentrasi reaktan akan menggeser kesetimbangan ke arah pembentukan produk, sehingga konsentrasi produk meningkat dan konsentrasi reaktan berkurang.
- Penambahan konsentrasi produk akan menggeser kesetimbangan ke arah pembentukan reaktan, sehingga konsentrasi reaktan meningkat dan konsentrasi produk berkurang.
- Pengurangan konsentrasi reaktan akan menggeser kesetimbangan ke arah pembentukan reaktan, sehingga konsentrasi reaktan meningkat dan konsentrasi produk berkurang.
- Pengurangan konsentrasi produk akan menggeser kesetimbangan ke arah pembentukan produk, sehingga konsentrasi produk meningkat dan konsentrasi reaktan berkurang.
Pengaruh Suhu terhadap Kesetimbangan
Suhu juga merupakan faktor penting yang dapat menggeser kesetimbangan reaksi.
- Pada reaksi endoterm, penambahan suhu akan menggeser kesetimbangan ke arah pembentukan produk, karena reaksi endoterm menyerap panas. Sebaliknya, penurunan suhu akan menggeser kesetimbangan ke arah pembentukan reaktan.
- Pada reaksi eksoterm, penambahan suhu akan menggeser kesetimbangan ke arah pembentukan reaktan, karena reaksi eksoterm melepaskan panas. Sebaliknya, penurunan suhu akan menggeser kesetimbangan ke arah pembentukan produk.
Pengaruh Tekanan terhadap Kesetimbangan
Perubahan tekanan hanya akan mempengaruhi kesetimbangan reaksi yang melibatkan gas.
- Peningkatan tekanan akan menggeser kesetimbangan ke arah reaksi yang menghasilkan lebih sedikit molekul gas. Sebaliknya, penurunan tekanan akan menggeser kesetimbangan ke arah reaksi yang menghasilkan lebih banyak molekul gas.
| Reaksi | Perubahan Tekanan | Pergeseran Kesetimbangan |
|---|---|---|
| N2(g) + 3H2(g) ⇌ 2NH3(g) | Peningkatan tekanan | Ke arah pembentukan amonia (NH3) |
| 2SO2(g) + O2(g) ⇌ 2SO3(g) | Penurunan tekanan | Ke arah pembentukan sulfur dioksida (SO2) dan oksigen (O2) |
Hukum Kesetimbangan
Dalam kimia, kesetimbangan merupakan keadaan di mana laju reaksi maju dan reaksi balik sama. Pada kondisi ini, konsentrasi reaktan dan produk tidak berubah seiring waktu. Hukum kesetimbangan menjelaskan hubungan antara konsentrasi reaktan dan produk pada saat kesetimbangan tercapai.
Konstanta Kesetimbangan (Kc dan Kp)
Konstanta kesetimbangan adalah nilai numerik yang menggambarkan rasio konsentrasi produk terhadap reaktan pada saat kesetimbangan. Ada dua jenis konstanta kesetimbangan, yaitu:
- Kc: Konstanta kesetimbangan yang dinyatakan dalam konsentrasi molar.
- Kp: Konstanta kesetimbangan yang dinyatakan dalam tekanan parsial.
Rumus untuk menghitung Kc dan Kp adalah:
Kc = [Produk]koefisien produk / [Reaktan]koefisien reaktan
Kp = (Pproduk)koefisien produk / (Preaktan)koefisien reaktan
di mana:
- [Produk] dan [Reaktan] adalah konsentrasi molar produk dan reaktan pada saat kesetimbangan.
- Pproduk dan Preaktan adalah tekanan parsial produk dan reaktan pada saat kesetimbangan.
- Koefisien produk dan reaktan adalah koefisien stoikiometri dalam persamaan reaksi seimbang.
Contoh Soal Menghitung Kc dan Kp
Perhatikan reaksi kesetimbangan berikut:
N2(g) + 3H2(g) ⇌ 2NH3(g)
Pada suhu tertentu, campuran gas N2, H2, dan NH3 mencapai kesetimbangan dengan konsentrasi berikut:
- [N2] = 0,1 M
- [H2] = 0,3 M
- [NH3] = 0,2 M
Hitunglah nilai Kc dan Kp untuk reaksi ini.
Penyelesaian:
Kc = [NH3]2 / [N2][H2]3 = (0,2)2 / (0,1)(0,3)3 = 7,41
Untuk menghitung Kp, kita perlu mengetahui tekanan parsial masing-masing gas. Jika kita asumsikan bahwa tekanan total sistem adalah 1 atm, maka tekanan parsial masing-masing gas dapat dihitung dengan hukum tekanan parsial Dalton:
- PN2 = (0,1 M / (0,1 + 0,3 + 0,2)) * 1 atm = 0,17 atm
- PH2 = (0,3 M / (0,1 + 0,3 + 0,2)) * 1 atm = 0,5 atm
- PNH3 = (0,2 M / (0,1 + 0,3 + 0,2)) * 1 atm = 0,33 atm
Kp = (PNH3)2 / (PN2)(PH2)3 = (0,33)2 / (0,17)(0,5)3 = 2,54
Hubungan Antara Kc dan Kp
Hubungan antara Kc dan Kp dapat dinyatakan dengan persamaan berikut:
Kp = Kc(RT)Δn
di mana:
- R adalah konstanta gas ideal (0,0821 L atm/mol K)
- T adalah suhu dalam Kelvin
- Δn adalah selisih koefisien stoikiometri produk dan reaktan dalam fase gas (Δn = jumlah mol gas produk – jumlah mol gas reaktan)
Persamaan ini menunjukkan bahwa Kc dan Kp memiliki nilai yang sama jika Δn = 0, yaitu jika jumlah mol gas produk sama dengan jumlah mol gas reaktan.
Prinsip Le Chatelier
Kesetimbangan kimia adalah keadaan di mana laju reaksi maju dan balik sama, sehingga konsentrasi reaktan dan produk tetap konstan. Namun, kesetimbangan ini bukanlah keadaan statis, melainkan keadaan dinamis. Prinsip Le Chatelier menjelaskan bagaimana kesetimbangan reaksi dapat berubah ketika terjadi perubahan kondisi, seperti perubahan suhu, tekanan, atau konsentrasi reaktan atau produk.
Prinsip Le Chatelier
Prinsip Le Chatelier menyatakan bahwa jika suatu sistem dalam kesetimbangan mengalami perubahan kondisi, maka sistem akan bergeser ke arah yang mengurangi efek perubahan tersebut. Artinya, jika terjadi perubahan kondisi yang dapat menggeser kesetimbangan, maka sistem akan bereaksi untuk mengurangi dampak perubahan tersebut dan mencapai kesetimbangan baru.
Aplikasi Prinsip Le Chatelier
Prinsip Le Chatelier dapat digunakan untuk memprediksi arah pergeseran kesetimbangan reaksi ketika terjadi perubahan kondisi. Berikut beberapa contoh aplikasi prinsip Le Chatelier:
- Perubahan Suhu:
- Jika reaksi eksotermis (melepaskan panas) dipanaskan, kesetimbangan akan bergeser ke arah kiri (reaksi balik) untuk menyerap panas dan mengurangi efek pemanasan.
- Jika reaksi endotermis (menyerap panas) didinginkan, kesetimbangan akan bergeser ke arah kiri (reaksi balik) untuk melepaskan panas dan mengurangi efek pendinginan.
- Perubahan Tekanan:
- Jika tekanan pada sistem reaksi ditingkatkan, kesetimbangan akan bergeser ke arah yang menghasilkan jumlah molekul gas yang lebih sedikit untuk mengurangi tekanan.
- Jika tekanan pada sistem reaksi diturunkan, kesetimbangan akan bergeser ke arah yang menghasilkan jumlah molekul gas yang lebih banyak untuk meningkatkan tekanan.
- Perubahan Konsentrasi:
- Jika konsentrasi reaktan ditingkatkan, kesetimbangan akan bergeser ke arah kanan (reaksi maju) untuk mengkonsumsi reaktan dan mencapai kesetimbangan baru.
- Jika konsentrasi produk ditingkatkan, kesetimbangan akan bergeser ke arah kiri (reaksi balik) untuk mengkonsumsi produk dan mencapai kesetimbangan baru.
Contoh Soal
Perhatikan reaksi kesetimbangan berikut:
N2(g) + 3H2(g) ⇌ 2NH3(g) ΔH = -92 kJ/mol
Reaksi ini merupakan reaksi eksotermis karena menghasilkan panas (ΔH negatif). Jika suhu reaksi ditingkatkan, maka kesetimbangan akan bergeser ke arah kiri (reaksi balik) untuk menyerap panas dan mengurangi efek pemanasan. Hal ini akan menyebabkan konsentrasi NH3 berkurang dan konsentrasi N2 dan H2 meningkat.
Pengaruh Katalis
Katalis adalah zat yang mempercepat laju reaksi tanpa dikonsumsi dalam reaksi tersebut. Katalis tidak mempengaruhi posisi kesetimbangan, tetapi hanya mempercepat tercapainya kesetimbangan. Katalis mempercepat laju reaksi maju dan balik secara sama, sehingga kesetimbangan tetap sama.
Soal Kesetimbangan Kimia
Kesetimbangan kimia merupakan kondisi di mana laju reaksi maju dan reaksi balik sama besar, sehingga konsentrasi reaktan dan produk tidak berubah secara makroskopis. Konsep kesetimbangan kimia sangat penting dalam memahami berbagai proses kimia, seperti pembentukan produk, efisiensi reaksi, dan prediksi arah reaksi.
Untuk menguji pemahamanmu tentang kesetimbangan kimia, berikut adalah contoh soal cerita yang bisa kamu coba selesaikan.
Soal Cerita Kesetimbangan Kimia
Soal-soal cerita tentang kesetimbangan kimia dapat membantu kita memahami bagaimana konsep ini diterapkan dalam berbagai situasi nyata. Berikut adalah tiga contoh soal cerita dengan tingkat kesulitan yang berbeda:
-
Soal 1 (Tingkat Kesulitan: Mudah)
Sebuah reaksi reversible sederhana adalah reaksi antara gas hidrogen (H2) dan gas iodin (I2) yang membentuk gas hidrogen iodida (HI). Jika kita memasukkan 1 mol H2 dan 1 mol I2 ke dalam wadah tertutup pada suhu tertentu, reaksi akan mencapai kesetimbangan. Pada saat kesetimbangan, terdapat 0,8 mol HI dalam wadah. Hitunglah nilai konstanta kesetimbangan (Kc) untuk reaksi ini.
-
Soal 2 (Tingkat Kesulitan: Sedang)
Reaksi pembentukan amonia (NH3) dari nitrogen (N2) dan hidrogen (H2) merupakan reaksi penting dalam industri pupuk. Reaksi ini berlangsung reversible dan dapat digambarkan sebagai berikut:
N2(g) + 3H2(g) ⇌ 2NH3(g)
Jika kita memasukkan 1 mol N2 dan 3 mol H2 ke dalam wadah tertutup pada suhu tertentu, reaksi akan mencapai kesetimbangan. Pada saat kesetimbangan, tekanan parsial NH3 adalah 2 atm. Hitunglah nilai konstanta kesetimbangan (Kp) untuk reaksi ini.
-
Soal 3 (Tingkat Kesulitan: Sulit)
Reaksi pembentukan karbon monoksida (CO) dari karbon (C) dan karbon dioksida (CO2) merupakan reaksi penting dalam industri logam. Reaksi ini berlangsung reversible dan dapat digambarkan sebagai berikut:
C(s) + CO2(g) ⇌ 2CO(g)
Jika kita memasukkan 1 mol CO2 ke dalam wadah tertutup yang berisi karbon padat pada suhu tertentu, reaksi akan mencapai kesetimbangan. Pada saat kesetimbangan, tekanan parsial CO adalah 1 atm. Hitunglah nilai konstanta kesetimbangan (Kp) untuk reaksi ini.
Tabel Soal dan Jawaban Kesetimbangan Kimia
Berikut adalah tabel yang berisi soal dan jawaban untuk berbagai jenis soal kesetimbangan kimia:
| No. | Soal | Jawaban |
|---|---|---|
| 1 | Hitunglah nilai Kc untuk reaksi berikut pada suhu tertentu: A(g) + B(g) ⇌ C(g) + D(g) Jika pada saat kesetimbangan konsentrasi A = 0,1 M, B = 0,2 M, C = 0,3 M, dan D = 0,4 M. |
Kc = [C][D] / [A][B] = (0,3)(0,4) / (0,1)(0,2) = 6 |
| 2 | Hitunglah nilai Kp untuk reaksi berikut pada suhu tertentu: 2SO2(g) + O2(g) ⇌ 2SO3(g) Jika pada saat kesetimbangan tekanan parsial SO2 = 1 atm, O2 = 2 atm, dan SO3 = 3 atm. |
Kp = (PSO3)2 / (PSO2)2(PO2) = (3)2 / (1)2(2) = 4,5 |
| 3 | Tentukan arah pergeseran kesetimbangan untuk reaksi berikut jika konsentrasi produk ditambah: N2(g) + 3H2(g) ⇌ 2NH3(g) |
Kesetimbangan akan bergeser ke kiri (reaksi balik) untuk mengurangi konsentrasi produk (NH3) dan mengembalikan kesetimbangan. |
| 4 | Tentukan arah pergeseran kesetimbangan untuk reaksi berikut jika suhu dinaikkan: 2NO2(g) ⇌ N2O4(g) ΔH = -58 kJ/mol |
Kesetimbangan akan bergeser ke kiri (reaksi balik) karena reaksi ini eksotermis (ΔH negatif). Menaikkan suhu akan menggeser kesetimbangan ke arah reaksi yang menyerap panas (reaksi endotermis). |
Contoh Soal Perhitungan Kc dan Kp dalam Kondisi Non-Standar
Perhitungan Kc dan Kp dapat dilakukan dalam kondisi non-standar (suhu dan tekanan tidak sama dengan kondisi standar). Dalam kasus ini, kita perlu menggunakan hukum kesetimbangan kimia dan informasi tentang perubahan entalpi dan entropi reaksi.
Misalnya, kita ingin menghitung nilai Kc untuk reaksi berikut pada suhu 500 K:
CO(g) + H2O(g) ⇌ CO2(g) + H2(g)
Pada suhu 298 K, nilai Kc untuk reaksi ini adalah 10. Perubahan entalpi standar (ΔH°) untuk reaksi ini adalah -41,2 kJ/mol, dan perubahan entropi standar (ΔS°) adalah -42,1 J/mol.K.
Untuk menghitung nilai Kc pada suhu 500 K, kita dapat menggunakan persamaan berikut:
ln(Kc500) – ln(Kc298) = -ΔH°/R (1/T500 – 1/T298)
Dimana:
- Kc500 adalah nilai Kc pada suhu 500 K.
- Kc298 adalah nilai Kc pada suhu 298 K (10).
- ΔH° adalah perubahan entalpi standar (-41,2 kJ/mol).
- R adalah konstanta gas ideal (8,314 J/mol.K).
- T500 adalah suhu dalam Kelvin (500 K).
- T298 adalah suhu dalam Kelvin (298 K).
Dengan memasukkan nilai-nilai yang diketahui ke dalam persamaan, kita dapat menghitung nilai Kc500.
Penerapan Kesetimbangan Kimia: Contoh Soal Ekuilibrium
Kesetimbangan kimia merupakan konsep penting dalam kimia yang menjelaskan keadaan di mana laju reaksi maju dan balik sama. Konsep ini tidak hanya berlaku dalam dunia laboratorium, tetapi juga memiliki aplikasi yang luas dalam berbagai bidang, seperti industri, kesehatan, dan lingkungan.
Penerapan Kesetimbangan Kimia dalam Industri
Kesetimbangan kimia memiliki peran penting dalam berbagai proses industri, khususnya dalam produksi bahan kimia. Salah satu contohnya adalah proses Haber-Bosch, sebuah proses penting dalam produksi amonia.
- Proses Haber-Bosch merupakan reaksi antara nitrogen dan hidrogen untuk menghasilkan amonia. Reaksi ini merupakan reaksi kesetimbangan, dan untuk mengoptimalkan hasil produksi amonia, diperlukan pemahaman yang mendalam tentang faktor-faktor yang memengaruhi kesetimbangan.
- Faktor-faktor yang memengaruhi kesetimbangan reaksi Haber-Bosch meliputi suhu, tekanan, dan konsentrasi reaktan. Dengan mengatur faktor-faktor ini, industri dapat memaksimalkan hasil produksi amonia dan meminimalkan biaya produksi.
Penerapan Kesetimbangan Kimia dalam Kesehatan
Kesetimbangan kimia juga berperan penting dalam menjaga kesehatan manusia. Banyak proses biokimia dalam tubuh melibatkan reaksi kesetimbangan.
- Contohnya, kesetimbangan asam-basa dalam darah sangat penting untuk menjaga fungsi organ tubuh. Asam dan basa dalam darah berada dalam kesetimbangan yang dinamis, dan perubahan kecil pada kesetimbangan ini dapat menyebabkan gangguan kesehatan, seperti asidosis atau alkalosis.
- Contoh soal: Seorang pasien mengalami asidosis metabolik, yaitu kondisi di mana darah menjadi terlalu asam. Untuk mengatasi kondisi ini, dokter dapat memberikan terapi dengan larutan bikarbonat, yang akan meningkatkan pH darah dan mengembalikan kesetimbangan asam-basa.
Penerapan Kesetimbangan Kimia dalam Lingkungan
Kesetimbangan kimia juga memiliki peran penting dalam menjaga keseimbangan lingkungan. Banyak reaksi kimia yang terjadi di lingkungan merupakan reaksi kesetimbangan.
- Contohnya, kesetimbangan karbon dioksida (CO2) di atmosfer. CO2 merupakan gas rumah kaca yang berperan dalam efek rumah kaca. Kesetimbangan CO2 di atmosfer dipengaruhi oleh berbagai faktor, seperti emisi dari pembakaran bahan bakar fosil dan penyerapan oleh tumbuhan.
- Contoh soal: Peningkatan emisi CO2 dari pembakaran bahan bakar fosil dapat mengganggu kesetimbangan CO2 di atmosfer, yang dapat menyebabkan peningkatan suhu global dan perubahan iklim.
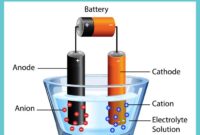
Kesetimbangan Ion
:max_bytes(150000):strip_icc()/Equilibrium_Final_4197021-7bf32e5137c34b37b8aac671535a1a25.jpg?w=700)
Kesetimbangan ion merupakan salah satu konsep penting dalam kimia yang menjelaskan tentang reaksi reversibel antara ion-ion dalam larutan. Konsep ini membantu kita memahami kelarutan garam, pembentukan endapan, dan berbagai reaksi kimia lainnya.
Pengertian Kesetimbangan Ion
Kesetimbangan ion terjadi ketika suatu garam larut dalam air, ion-ion penyusun garam tersebut akan terdisosiasi dan berada dalam kesetimbangan dengan garam yang tidak terlarut. Kesetimbangan ini dikontrol oleh suatu konstanta kesetimbangan yang disebut dengan konstanta hasil kali kelarutan (Ksp). Ksp merupakan ukuran kelarutan suatu garam. Semakin besar nilai Ksp, maka semakin besar kelarutan garam tersebut.
Sebagai contoh, ketika garam AgCl dilarutkan dalam air, terjadi kesetimbangan antara ion Ag+ dan Cl- dengan garam AgCl yang tidak terlarut:
AgCl(s) <=> Ag+(aq) + Cl-(aq)
Kesetimbangan ini menunjukkan bahwa sebagian kecil garam AgCl terlarut dan membentuk ion Ag+ dan Cl- dalam larutan, sementara sebagian lainnya tetap dalam bentuk padatan. Pada keadaan setimbang, laju pelarutan AgCl sama dengan laju pengendapan ion Ag+ dan Cl- menjadi AgCl.
Hubungan antara Ksp dan Kelarutan
Ksp dan kelarutan suatu garam memiliki hubungan yang erat. Berikut adalah tabel yang menunjukkan hubungan tersebut:
| Ksp | Kelarutan |
|---|---|
| Ksp kecil | Kelarutan rendah |
| Ksp besar | Kelarutan tinggi |
Pada tabel di atas, dapat disimpulkan bahwa semakin kecil nilai Ksp, maka semakin rendah kelarutan garam tersebut. Sebaliknya, semakin besar nilai Ksp, maka semakin tinggi kelarutan garam tersebut.
Contoh Soal Perhitungan Ksp dan Kelarutan
Berikut adalah contoh soal yang melibatkan perhitungan Ksp dan kelarutan:
Soal:
Kelarutan AgCl dalam air adalah 1,3 x 10^-5 mol/L. Hitunglah Ksp AgCl.
Penyelesaian:
AgCl(s) <=> Ag+(aq) + Cl-(aq)
Kelarutan AgCl = [Ag+] = [Cl-] = 1,3 x 10^-5 mol/L
Ksp = [Ag+][Cl-] = (1,3 x 10^-5 mol/L) x (1,3 x 10^-5 mol/L) = 1,69 x 10^-10
Jadi, Ksp AgCl adalah 1,69 x 10^-10.
Kesetimbangan Asam Basa
Kesetimbangan asam basa merupakan konsep penting dalam kimia yang menjelaskan interaksi antara asam dan basa dalam larutan. Konsep ini mendasari pemahaman kita tentang pH larutan, sifat asam dan basa, serta bagaimana reaksi kimia terjadi dalam larutan. Kesetimbangan asam basa memainkan peran vital dalam berbagai bidang, termasuk kimia, biologi, kedokteran, dan lingkungan.
Pengertian Kesetimbangan Asam Basa
Kesetimbangan asam basa terjadi ketika asam dan basa bereaksi secara reversibel dalam larutan. Reaksi ini menghasilkan ion hidronium (H3O+) dan ion hidroksida (OH–). Kesetimbangan asam basa dapat digambarkan dengan persamaan reaksi berikut:
HA + H2O ⇌ H3O+ + A–
Dimana HA adalah asam lemah, A– adalah basa konjugat dari asam tersebut, dan H2O adalah pelarut. Dalam kesetimbangan, laju reaksi maju dan reaksi balik sama, sehingga konsentrasi reaktan dan produk tetap konstan.
Contoh Kesetimbangan Asam Basa
Contoh kesetimbangan asam basa dapat diilustrasikan dengan reaksi antara asam asetat (CH3COOH) dan air. Asam asetat merupakan asam lemah yang bereaksi dengan air untuk menghasilkan ion hidronium (H3O+) dan ion asetat (CH3COO–). Kesetimbangan ini dapat ditulis sebagai berikut:
CH3COOH + H2O ⇌ H3O+ + CH3COO–
Dalam larutan, asam asetat sebagian terionisasi menjadi ion hidronium dan ion asetat. Kesetimbangan ini menunjukkan bahwa larutan asam asetat mengandung asam asetat yang tidak terionisasi, ion hidronium, dan ion asetat.
Nilai Ka dan Kb untuk Asam dan Basa Lemah
Nilai Ka dan Kb merupakan konstanta kesetimbangan yang menunjukkan kekuatan asam dan basa lemah. Nilai Ka menunjukkan kecenderungan asam untuk melepaskan ion hidronium (H3O+), sedangkan nilai Kb menunjukkan kecenderungan basa untuk menerima ion hidronium (H3O+). Semakin besar nilai Ka, semakin kuat asam tersebut. Sebaliknya, semakin besar nilai Kb, semakin kuat basa tersebut.
| Asam/Basa | Rumus | Ka | Kb |
|---|---|---|---|
| Asam asetat | CH3COOH | 1.8 x 10-5 | 5.6 x 10-10 |
| Asam benzoat | C6H5COOH | 6.3 x 10-5 | 1.6 x 10-10 |
| Amonia | NH3 | – | 1.8 x 10-5 |
| Metilamin | CH3NH2 | – | 4.4 x 10-4 |
Tabel di atas menunjukkan nilai Ka dan Kb untuk beberapa asam dan basa lemah. Dapat dilihat bahwa asam asetat dan asam benzoat merupakan asam lemah, sedangkan amonia dan metilamin merupakan basa lemah.
Contoh Soal Perhitungan pH Larutan Buffer
Larutan buffer adalah larutan yang dapat menahan perubahan pH ketika ditambahkan asam atau basa. Larutan buffer biasanya terdiri dari asam lemah dan basa konjugatnya, atau basa lemah dan asam konjugatnya. Berikut adalah contoh soal perhitungan pH larutan buffer:
Hitung pH larutan buffer yang terdiri dari 0.1 M asam asetat (CH3COOH) dan 0.1 M natrium asetat (CH3COONa). Diketahui Ka asam asetat = 1.8 x 10-5.
Contoh soal ekuilibrium seringkali membahas tentang penentuan kondisi kesetimbangan suatu reaksi kimia. Misalnya, soal bisa meminta kita untuk menentukan konsentrasi zat-zat pada saat kesetimbangan tercapai. Nah, untuk menyelesaikan soal-soal seperti ini, kita perlu memahami konsep pergeseran kesetimbangan, yang juga dibahas dalam contoh soal menyusul.
Konsep ini penting untuk menentukan bagaimana perubahan kondisi reaksi, seperti penambahan produk atau reaktan, akan mempengaruhi posisi kesetimbangan. Dengan memahami kedua konsep ini, kamu akan lebih siap menghadapi berbagai jenis soal ekuilibrium.
Untuk menghitung pH larutan buffer, kita dapat menggunakan persamaan Henderson-Hasselbalch:
pH = pKa + log ([basa]/[asam])
Dimana:
- pKa = -log Ka = -log (1.8 x 10-5) = 4.74
- [basa] = konsentrasi basa konjugat = 0.1 M
- [asam] = konsentrasi asam lemah = 0.1 M
Dengan demikian, pH larutan buffer dapat dihitung sebagai berikut:
pH = 4.74 + log (0.1/0.1) = 4.74
Jadi, pH larutan buffer adalah 4.74.
Kesetimbangan Heterogen
Kesetimbangan heterogen merupakan suatu keadaan kesetimbangan yang terjadi dalam sistem reaksi yang melibatkan lebih dari satu fase. Misalnya, reaksi antara zat padat dan gas, atau reaksi antara zat cair dan gas. Pada kesetimbangan heterogen, konsentrasi zat-zat dalam fase yang berbeda tidak selalu sama.
Perbedaan Kesetimbangan Homogen dan Heterogen
Perbedaan antara kesetimbangan homogen dan heterogen dapat diringkas dalam tabel berikut:
| Aspek | Kesetimbangan Homogen | Kesetimbangan Heterogen |
|---|---|---|
| Fase | Semua reaktan dan produk berada dalam fase yang sama | Reaktan dan produk berada dalam fase yang berbeda |
| Contoh | Reaksi antara gas, reaksi antara zat cair | Reaksi antara zat padat dan gas, reaksi antara zat cair dan gas |
| Rumus Kc dan Kp | Kc dan Kp hanya melibatkan konsentrasi atau tekanan parsial zat-zat dalam fase yang sama | Kc dan Kp hanya melibatkan konsentrasi atau tekanan parsial zat-zat dalam fase yang sama, tidak melibatkan zat padat atau zat cair murni |
Contoh Soal Kesetimbangan Heterogen, Contoh soal ekuilibrium
Berikut adalah contoh soal yang melibatkan perhitungan Kc dan Kp untuk kesetimbangan heterogen:
Reaksi penguraian kalsium karbonat (CaCO3) menjadi kalsium oksida (CaO) dan karbon dioksida (CO2) merupakan contoh kesetimbangan heterogen:
CaCO3(s) ⇌ CaO(s) + CO2(g)
Jika pada suhu tertentu, tekanan parsial CO2 dalam kesetimbangan adalah 0,5 atm, tentukan nilai Kp untuk reaksi tersebut.
Penyelesaian:
Kp = P(CO2) = 0,5 atm
Jadi, nilai Kp untuk reaksi penguraian kalsium karbonat pada suhu tersebut adalah 0,5 atm.
Kesimpulan
Melalui contoh soal ekuilibrium, kita dapat melihat bagaimana konsep ini diterapkan dalam berbagai bidang, mulai dari industri kimia hingga kesehatan dan lingkungan. Memahami kesetimbangan kimia tidak hanya penting untuk menyelesaikan soal-soal, tetapi juga untuk memahami bagaimana reaksi kimia bekerja dan bagaimana kita dapat memanipulasinya untuk mencapai hasil yang diinginkan.