Contoh soal kekekalan massa – Pernahkah kamu bertanya-tanya mengapa bahan makanan yang kita masak tidak menghilang begitu saja? Atau bagaimana pabrik kimia menghasilkan produk dengan memanfaatkan bahan baku tertentu? Jawabannya terletak pada konsep kekekalan massa, sebuah prinsip fundamental dalam ilmu kimia yang menyatakan bahwa massa total zat sebelum dan sesudah reaksi kimia selalu sama. Konsep ini mungkin terdengar sederhana, namun memiliki implikasi yang luas dalam berbagai bidang ilmu pengetahuan dan teknologi.
Dalam artikel ini, kita akan menjelajahi konsep kekekalan massa dengan membahas definisi, hukum, penerapan, dan contoh soal yang menguji pemahamanmu tentang topik ini. Kita juga akan melihat bagaimana prinsip ini berperan penting dalam kehidupan sehari-hari, mulai dari proses memasak hingga industri kimia.
Pengertian Kekekalan Massa
Kekekalan massa merupakan konsep dasar dalam ilmu kimia yang menyatakan bahwa massa total zat-zat yang terlibat dalam reaksi kimia tetap sama, baik sebelum maupun sesudah reaksi berlangsung. Konsep ini didasarkan pada prinsip bahwa materi tidak dapat diciptakan atau dimusnahkan, hanya dapat diubah bentuknya.
Ilustrasi Sederhana Kekekalan Massa
Bayangkan Anda mencampur tepung, gula, dan telur untuk membuat adonan kue. Massa total bahan-bahan ini, yaitu tepung, gula, dan telur, akan sama dengan massa adonan kue yang dihasilkan. Meskipun bahan-bahan ini telah mengalami perubahan bentuk dan komposisi, massa totalnya tetap sama.
Perbandingan Massa Reaktan dan Produk dalam Reaksi Kimia
Berikut adalah tabel yang menunjukkan perbandingan massa reaktan dan produk dalam reaksi kimia sederhana:
| Reaktan | Massa (gram) | Produk | Massa (gram) |
|---|---|---|---|
| Hidrogen (H2) | 2 | Air (H2O) | 18 |
| Oksigen (O2) | 16 | ||
| Total | 18 | Total | 18 |
Dari tabel di atas, dapat dilihat bahwa massa total reaktan (hidrogen dan oksigen) sama dengan massa total produk (air). Hal ini menunjukkan bahwa dalam reaksi kimia, massa tidak hilang atau bertambah, melainkan hanya berubah bentuk.
Hukum Kekekalan Massa: Contoh Soal Kekekalan Massa
Hukum kekekalan massa merupakan salah satu hukum dasar dalam kimia yang menjelaskan bahwa massa dalam sistem tertutup tidak akan berubah, baik sebelum, selama, maupun setelah reaksi kimia terjadi. Konsep ini mendasari pemahaman kita tentang bagaimana materi berubah dan berinteraksi dalam berbagai proses kimia dan fisika.
Pernyataan Hukum Kekekalan Massa
Hukum kekekalan massa menyatakan bahwa dalam sistem tertutup, total massa reaktan (zat yang bereaksi) akan sama dengan total massa produk (zat yang dihasilkan) setelah reaksi kimia selesai. Dengan kata lain, massa tidak dapat diciptakan atau dimusnahkan, hanya dapat diubah bentuknya.
Penemu Hukum Kekekalan Massa
Hukum kekekalan massa pertama kali dirumuskan oleh seorang ilmuwan Perancis bernama Antoine Lavoisier pada tahun 1789. Lavoisier melakukan percobaan dengan membakar logam timbal dalam wadah tertutup. Ia menemukan bahwa massa timbal dan oksigen sebelum pembakaran sama dengan massa timbal oksida yang dihasilkan setelah pembakaran. Berdasarkan hasil percobaannya, Lavoisier menyimpulkan bahwa massa total zat sebelum dan sesudah reaksi kimia tetap sama.
Implikasi Hukum Kekekalan Massa
Hukum kekekalan massa memiliki implikasi yang luas dalam berbagai bidang ilmu pengetahuan, termasuk:
- Kimia: Hukum ini membantu kita untuk memahami bagaimana reaksi kimia terjadi dan bagaimana massa zat berubah selama reaksi. Misalnya, dalam reaksi pembakaran, massa kayu yang terbakar akan sama dengan massa abu, gas karbon dioksida, dan uap air yang dihasilkan.
- Fisika: Hukum kekekalan massa merupakan salah satu hukum dasar fisika yang terkait dengan konsep kekekalan energi. Dalam sistem tertutup, energi total, termasuk massa, akan tetap konstan.
- Biologi: Hukum kekekalan massa membantu kita untuk memahami bagaimana organisme hidup memperoleh dan menggunakan energi. Misalnya, dalam proses fotosintesis, tumbuhan menggunakan energi cahaya matahari untuk mengubah karbon dioksida dan air menjadi glukosa dan oksigen. Massa total zat sebelum dan sesudah fotosintesis tetap sama.
- Teknik: Hukum kekekalan massa digunakan dalam berbagai aplikasi teknik, seperti dalam desain reaktor kimia, perancangan sistem pembuangan limbah, dan analisis siklus hidup produk.
Penerapan Kekekalan Massa
Kekekalan massa merupakan prinsip fundamental dalam kimia yang menyatakan bahwa massa total zat-zat yang terlibat dalam reaksi kimia tetap konstan, baik sebelum maupun setelah reaksi. Artinya, dalam reaksi kimia, massa tidak hilang atau muncul begitu saja, melainkan hanya berubah bentuk. Prinsip ini memiliki aplikasi luas dalam berbagai bidang, termasuk kimia, fisika, dan ilmu lingkungan.
Contoh Soal Kekekalan Massa
Kekekalan massa dapat diuji dengan berbagai contoh soal. Berikut adalah salah satu contohnya:
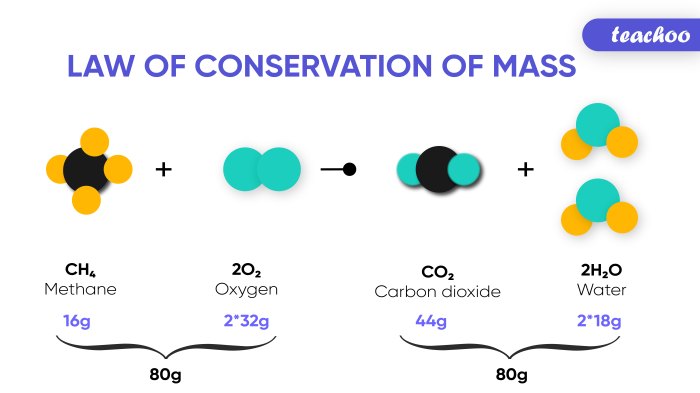
- Misalnya, dalam reaksi pembakaran metana (CH4) dengan oksigen (O2) menghasilkan karbon dioksida (CO2) dan air (H2O). Reaksi ini dapat ditulis sebagai berikut:
- Jika kita membakar 16 gram metana dengan 64 gram oksigen, maka berdasarkan hukum kekekalan massa, total massa produk reaksi (karbon dioksida dan air) harus sama dengan total massa reaktan (metana dan oksigen).
- Massa karbon dioksida yang dihasilkan adalah 44 gram dan massa air yang dihasilkan adalah 36 gram. Total massa produk (44 gram + 36 gram) sama dengan total massa reaktan (16 gram + 64 gram), yaitu 80 gram. Ini membuktikan bahwa massa total sebelum dan sesudah reaksi tetap sama.
CH4 + 2O2 → CO2 + 2H2O
Cara Menghitung Massa Produk Reaksi
Untuk menghitung massa produk reaksi kimia dengan menerapkan hukum kekekalan massa, kita dapat menggunakan persamaan berikut:
Massa reaktan = Massa produk
Langkah-langkah yang dapat digunakan adalah:
- Tentukan massa reaktan yang terlibat dalam reaksi.
- Tentukan massa produk yang dihasilkan dari reaksi.
- Jumlahkan massa reaktan dan massa produk.
- Jika massa reaktan sama dengan massa produk, maka hukum kekekalan massa terpenuhi.
Penerapan Kekekalan Massa dalam Proses Industri Kimia
Prinsip kekekalan massa memiliki aplikasi yang luas dalam berbagai proses industri kimia, antara lain:
- Perhitungan Stoikiometri: Kekekalan massa digunakan untuk menentukan jumlah reaktan dan produk yang diperlukan dalam suatu reaksi kimia, sehingga dapat memaksimalkan efisiensi proses dan meminimalkan pemborosan.
- Kontrol Proses: Dalam proses industri, kekekalan massa digunakan untuk memonitor dan mengontrol aliran material, memastikan bahwa tidak ada kehilangan atau penambahan massa yang tidak terduga. Ini penting untuk menjaga kualitas produk dan efisiensi proses.
- Analisis Lingkungan: Kekekalan massa digunakan untuk menganalisis aliran material dalam sistem lingkungan, seperti aliran air, udara, dan tanah. Ini membantu dalam memahami siklus material dan dampak lingkungan dari berbagai aktivitas manusia.
Contoh Soal dan Pembahasan
Setelah memahami konsep kekekalan massa, mari kita lihat penerapannya dalam reaksi kimia sederhana melalui contoh soal dan pembahasannya.
Contoh Soal Kekekalan Massa
Perhatikan reaksi kimia sederhana berikut:
A + B → C + D
Dimana:
- A dan B adalah reaktan (zat yang bereaksi)
- C dan D adalah produk (zat yang dihasilkan)
Misalkan massa A = 10 gram, massa B = 5 gram, dan massa C = 8 gram. Berapakah massa D?
Pembahasan
Berdasarkan hukum kekekalan massa, total massa reaktan harus sama dengan total massa produk. Dengan kata lain:
Massa A + Massa B = Massa C + Massa D
Maka, untuk menghitung massa D, kita dapat menggunakan rumus:
Massa D = (Massa A + Massa B) – Massa C
Substitusikan nilai yang diketahui:
Massa D = (10 gram + 5 gram) – 8 gram
Massa D = 15 gram – 8 gram
Massa D = 7 gram
Tabel Data Massa, Contoh soal kekekalan massa
| Zat | Massa (gram) |
|---|---|
| A | 10 |
| B | 5 |
| C | 8 |
| D | 7 |
Dari tabel di atas, terlihat bahwa total massa reaktan (A + B = 15 gram) sama dengan total massa produk (C + D = 15 gram). Ini membuktikan bahwa hukum kekekalan massa berlaku dalam reaksi kimia ini.
Contoh soal kekekalan massa biasanya melibatkan reaksi kimia, di mana total massa reaktan sama dengan total massa produk. Misalnya, reaksi pembakaran kayu menghasilkan abu, asap, dan gas, namun total massa sebelum dan sesudah pembakaran tetap sama. Konsep ini juga bisa diterapkan dalam berbagai bidang, seperti dalam contoh soal essay konflik sosial dan jawaban yang membahas tentang konflik sosial dan solusi penyelesaiannya.
Memahami konsep kekekalan massa penting untuk memahami berbagai fenomena alam dan proses kimia di sekitar kita.
Percobaan Kekekalan Massa
Hukum kekekalan massa menyatakan bahwa dalam sistem tertutup, massa total zat sebelum dan sesudah reaksi kimia atau perubahan fisika akan selalu sama. Artinya, massa tidak dapat diciptakan atau dimusnahkan, hanya diubah bentuknya. Untuk membuktikan hukum ini, kita dapat melakukan percobaan sederhana di rumah atau di laboratorium.
Percobaan Sederhana Kekekalan Massa
Percobaan ini melibatkan reaksi kimia sederhana antara asam cuka (CH3COOH) dan natrium bikarbonat (NaHCO3) untuk menghasilkan karbon dioksida (CO2), air (H2O), dan garam (CH3COONa). Percobaan ini bertujuan untuk menunjukkan bahwa massa total zat sebelum dan sesudah reaksi tetap sama, meskipun terjadi perubahan bentuk dan wujud.
- Bahan yang Dibutuhkan:
- Asam cuka (CH3COOH)
- Natrium bikarbonat (NaHCO3)
- Gelas kimia atau wadah transparan
- Timbangan
- Langkah-langkah Percobaan:
- Timbang asam cuka dan natrium bikarbonat secara terpisah. Catat massanya.
- Masukkan asam cuka ke dalam gelas kimia.
- Tambahkan natrium bikarbonat secara perlahan ke dalam asam cuka. Perhatikan reaksi yang terjadi, seperti timbulnya gelembung gas karbon dioksida.
- Tunggu hingga reaksi selesai dan semua gelembung gas berhenti muncul.
- Timbang kembali isi gelas kimia. Catat massanya.
Ilustrasi Percobaan
Dalam ilustrasi percobaan, kita dapat melihat perubahan massa reaktan dan produk. Sebelum reaksi, kita memiliki massa asam cuka dan natrium bikarbonat. Setelah reaksi, kita memiliki massa karbon dioksida, air, dan garam. Meskipun terjadi perubahan bentuk dan wujud, massa total zat sebelum dan sesudah reaksi tetap sama. Ini menunjukkan bahwa massa tidak dapat diciptakan atau dimusnahkan, hanya diubah bentuknya.
Massa reaktan = Massa produk
Contohnya, jika kita memiliki 10 gram asam cuka dan 5 gram natrium bikarbonat, maka total massa reaktan adalah 15 gram. Setelah reaksi, kita akan mendapatkan 15 gram karbon dioksida, air, dan garam. Massa total tetap 15 gram, meskipun terjadi perubahan bentuk dan wujud.
Simpulan Akhir
Memahami konsep kekekalan massa tidak hanya penting dalam dunia ilmu pengetahuan, tetapi juga dalam kehidupan sehari-hari. Dengan memahami prinsip ini, kita dapat lebih menghargai bagaimana alam bekerja dan bagaimana kita dapat memanfaatkannya untuk mencapai tujuan yang lebih baik. Jadi, mari kita terus belajar dan menjelajahi keajaiban ilmu kimia!