Contoh soal perubahan entalpi reaksi dan pembahasannya – Pernahkah kamu bertanya-tanya mengapa reaksi kimia tertentu melepaskan panas, sementara yang lain menyerap panas? Nah, konsep perubahan entalpi reaksi akan membantu kita memahami hal ini! Perubahan entalpi reaksi merupakan perubahan energi yang terjadi dalam suatu reaksi kimia, yang dapat berupa pelepasan atau penyerapan panas. Dalam artikel ini, kita akan menjelajahi konsep perubahan entalpi reaksi melalui contoh soal dan pembahasannya.
Perubahan entalpi reaksi dipengaruhi oleh berbagai faktor, seperti suhu, tekanan, dan konsentrasi. Kita juga akan membahas hukum Hess yang membantu kita menghitung perubahan entalpi reaksi dengan menggunakan data reaksi lain. Selain itu, kita akan mempelajari entalpi pembentukan standar, entalpi pembakaran standar, dan entalpi ikatan, yang semuanya memberikan informasi penting tentang perubahan energi dalam reaksi kimia.
Pengertian Perubahan Entalpi Reaksi
Perubahan entalpi reaksi merupakan salah satu konsep penting dalam kimia yang berkaitan dengan perubahan energi yang terjadi selama reaksi kimia. Entalpi sendiri merupakan jumlah energi internal suatu sistem ditambah dengan hasil kali tekanan dan volumenya. Dalam reaksi kimia, perubahan entalpi menunjukkan perubahan energi yang menyertai perubahan keadaan zat.
Pengertian Perubahan Entalpi Reaksi
Perubahan entalpi reaksi, dilambangkan dengan ΔH, didefinisikan sebagai perubahan jumlah energi yang terjadi ketika reaksi kimia berlangsung pada tekanan tetap. ΔH dapat bernilai positif atau negatif, tergantung pada apakah energi dilepaskan atau diserap selama reaksi.
Jenis-jenis Perubahan Entalpi Reaksi
Perubahan entalpi reaksi diklasifikasikan berdasarkan jenis reaksi yang terjadi, berikut adalah beberapa jenis perubahan entalpi reaksi:
- Entalpi pembentukan standar (ΔHf°): Perubahan entalpi yang terjadi ketika satu mol senyawa dibentuk dari unsur-unsurnya dalam keadaan standar (suhu 298 K dan tekanan 1 atm).
- Entalpi pembakaran standar (ΔHc°): Perubahan entalpi yang terjadi ketika satu mol zat terbakar sempurna dalam keadaan standar.
- Entalpi penguraian standar (ΔHd°): Perubahan entalpi yang terjadi ketika satu mol senyawa terurai menjadi unsur-unsurnya dalam keadaan standar.
- Entalpi pelarutan standar (ΔHs°): Perubahan entalpi yang terjadi ketika satu mol zat terlarut dilarutkan dalam pelarut dalam keadaan standar.
- Entalpi netralisasi standar (ΔHn°): Perubahan entalpi yang terjadi ketika satu mol asam direaksikan dengan satu mol basa dalam keadaan standar.
Contoh Reaksi Kimia dengan Entalpi Positif dan Negatif
Perubahan entalpi reaksi dapat dibedakan menjadi dua jenis berdasarkan perubahan energinya:
- Reaksi endoterm: Reaksi yang menyerap energi dari lingkungan, sehingga ΔH bernilai positif. Contohnya, reaksi penguraian kalsium karbonat menjadi kalsium oksida dan karbon dioksida.
CaCO3(s) + energi → CaO(s) + CO2(g)
- Reaksi eksoterm: Reaksi yang melepaskan energi ke lingkungan, sehingga ΔH bernilai negatif. Contohnya, reaksi pembakaran metana menghasilkan karbon dioksida dan air.
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) + energi
Faktor-Faktor yang Mempengaruhi Perubahan Entalpi Reaksi
Perubahan entalpi reaksi, yang merupakan perubahan energi panas yang terjadi selama reaksi kimia, dipengaruhi oleh berbagai faktor. Pemahaman mengenai faktor-faktor ini sangat penting untuk mengendalikan dan memprediksi perubahan energi yang terjadi dalam suatu reaksi.
Pengaruh Suhu
Suhu merupakan faktor yang sangat berpengaruh terhadap perubahan entalpi reaksi. Secara umum, peningkatan suhu akan meningkatkan energi kinetik molekul reaktan, sehingga lebih mudah untuk mencapai keadaan transisi dan memicu reaksi. Hal ini akan menyebabkan perubahan entalpi reaksi menjadi lebih besar, baik positif (reaksi endotermik) maupun negatif (reaksi eksotermik).
Pengaruh Tekanan
Tekanan memiliki pengaruh yang signifikan terhadap perubahan entalpi reaksi, terutama pada reaksi yang melibatkan gas. Peningkatan tekanan akan menyebabkan molekul gas saling berdekatan, sehingga meningkatkan frekuensi tumbukan dan mempercepat reaksi. Untuk reaksi yang melibatkan gas, peningkatan tekanan umumnya akan meningkatkan perubahan entalpi reaksi, baik positif maupun negatif.
Pengaruh Konsentrasi
Konsentrasi reaktan juga memiliki pengaruh yang signifikan terhadap perubahan entalpi reaksi. Peningkatan konsentrasi reaktan akan meningkatkan frekuensi tumbukan antar molekul, sehingga mempercepat reaksi. Hal ini akan menyebabkan perubahan entalpi reaksi menjadi lebih besar, baik positif maupun negatif.
Contoh Perhitungan Perubahan Entalpi Reaksi
Sebagai contoh, perhatikan reaksi pembakaran metana:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
Perubahan entalpi reaksi ini akan dipengaruhi oleh faktor-faktor seperti suhu, tekanan, dan konsentrasi reaktan. Misalnya, jika suhu reaksi ditingkatkan, maka perubahan entalpi reaksi akan menjadi lebih besar (lebih negatif), karena reaksi pembakaran metana merupakan reaksi eksotermik. Begitu pula, jika tekanan reaksi ditingkatkan, maka perubahan entalpi reaksi akan menjadi lebih besar, karena reaksi ini melibatkan gas.
Ilustrasi Diagram
Berikut adalah ilustrasi diagram yang menunjukkan hubungan antara faktor-faktor yang mempengaruhi perubahan entalpi reaksi dengan contoh konkret:
Gambar:
Diagram menunjukkan perubahan entalpi reaksi pembakaran metana (CH4) pada berbagai suhu. Pada suhu rendah, perubahan entalpi reaksi relatif kecil, tetapi semakin tinggi suhu, perubahan entalpi reaksi menjadi lebih besar (lebih negatif). Hal ini menunjukkan bahwa peningkatan suhu akan meningkatkan laju reaksi dan melepaskan lebih banyak energi panas.
Hukum Hess

Hukum Hess adalah salah satu hukum dasar dalam termokimia yang membahas tentang hubungan antara perubahan entalpi reaksi dengan reaksi-reaksi lain yang terkait. Hukum ini menyatakan bahwa perubahan entalpi reaksi adalah sama, baik reaksi tersebut berlangsung dalam satu tahap atau dalam beberapa tahap. Hukum ini sangat berguna dalam menentukan perubahan entalpi reaksi yang sulit atau tidak mungkin diukur secara langsung.
Pengertian Hukum Hess
Hukum Hess menyatakan bahwa perubahan entalpi suatu reaksi tidak bergantung pada jalur reaksi yang ditempuh, tetapi hanya bergantung pada keadaan awal dan keadaan akhir reaksi. Dengan kata lain, perubahan entalpi reaksi adalah besaran keadaan yang tidak bergantung pada jalur reaksi.
Penerapan Hukum Hess
Hukum Hess dapat diterapkan untuk menghitung perubahan entalpi reaksi yang sulit diukur secara langsung dengan menggunakan data perubahan entalpi reaksi lain yang sudah diketahui. Berikut adalah langkah-langkah yang dapat dilakukan dalam menerapkan Hukum Hess:
| Langkah | Penjelasan |
|---|---|
| 1. Tuliskan persamaan reaksi yang ingin diketahui perubahan entalpinya. | Tentukan reaksi yang ingin Anda hitung perubahan entalpinya. |
| 2. Carilah persamaan reaksi yang sudah diketahui perubahan entalpinya, yang melibatkan reaktan dan produk reaksi yang ingin Anda hitung. | Anda perlu menemukan reaksi-reaksi yang sudah diketahui perubahan entalpinya dan melibatkan reaktan dan produk yang sama dengan reaksi yang ingin Anda hitung. |
| 3. Manipulasi persamaan reaksi yang sudah diketahui, sehingga reaktan dan produknya sesuai dengan persamaan reaksi yang ingin Anda hitung. | Anda mungkin perlu membalikkan persamaan reaksi, mengalikannya dengan faktor tertentu, atau menggabungkannya untuk mendapatkan persamaan reaksi yang ingin Anda hitung. |
| 4. Hitung perubahan entalpi reaksi yang ingin Anda hitung, dengan menggunakan perubahan entalpi reaksi yang sudah diketahui dan manipulasi yang dilakukan pada persamaan reaksi. | Perubahan entalpi reaksi yang ingin Anda hitung sama dengan jumlah perubahan entalpi reaksi yang sudah diketahui, dengan mempertimbangkan manipulasi yang dilakukan pada persamaan reaksi. |
Contoh Soal Penerapan Hukum Hess
Misalnya, kita ingin menentukan perubahan entalpi reaksi pembakaran metana (CH4) menjadi karbon dioksida (CO2) dan air (H2O) seperti persamaan reaksi berikut:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
Reaksi ini sulit diukur secara langsung. Namun, kita dapat menggunakan data perubahan entalpi reaksi lain yang sudah diketahui untuk menentukan perubahan entalpi reaksi pembakaran metana. Berikut adalah data perubahan entalpi reaksi yang sudah diketahui:
C(s) + O2(g) → CO2(g) ΔH = -393,5 kJ/mol
H2(g) + 1/2O2(g) → H2O(l) ΔH = -285,8 kJ/mol
C(s) + 2H2(g) → CH4(g) ΔH = -74,8 kJ/mol
Untuk mendapatkan persamaan reaksi pembakaran metana, kita dapat melakukan manipulasi pada persamaan reaksi yang sudah diketahui. Pertama, kita balikkan persamaan reaksi ketiga:
CH4(g) → C(s) + 2H2(g) ΔH = +74,8 kJ/mol
Kemudian, kita kalikan persamaan reaksi pertama dengan 1 dan persamaan reaksi kedua dengan 2:
C(s) + O2(g) → CO2(g) ΔH = -393,5 kJ/mol
2H2(g) + O2(g) → 2H2O(l) ΔH = -571,6 kJ/mol
Setelah itu, kita jumlahkan ketiga persamaan reaksi tersebut:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) ΔH = -890,3 kJ/mol
Jadi, perubahan entalpi reaksi pembakaran metana adalah -890,3 kJ/mol.
Entalpi Pembentukan Standar
Entalpi pembentukan standar adalah perubahan entalpi yang terjadi ketika satu mol senyawa dibentuk dari unsur-unsurnya dalam keadaan standar. Keadaan standar didefinisikan sebagai suhu 298 K (25 °C) dan tekanan 1 atm.
Pengertian Entalpi Pembentukan Standar
Entalpi pembentukan standar dilambangkan dengan ΔHf°. Nilai entalpi pembentukan standar dapat positif atau negatif. Entalpi pembentukan standar positif menunjukkan bahwa reaksi pembentukan senyawa tersebut bersifat endotermik, yaitu membutuhkan energi untuk berlangsung. Sebaliknya, entalpi pembentukan standar negatif menunjukkan bahwa reaksi pembentukan senyawa tersebut bersifat eksotermik, yaitu melepaskan energi ke lingkungan.
Sebagai contoh konkret, entalpi pembentukan standar air (H2O) adalah -285,8 kJ/mol. Ini berarti bahwa ketika 1 mol air dibentuk dari unsur-unsurnya, yaitu hidrogen (H2) dan oksigen (O2), dalam keadaan standar, akan dilepaskan energi sebesar 285,8 kJ.
Tabel Entalpi Pembentukan Standar
Berikut adalah tabel yang berisi data entalpi pembentukan standar untuk berbagai senyawa:
| Senyawa | ΔHf° (kJ/mol) |
|---|---|
| H2O(l) | -285,8 |
| CO2(g) | -393,5 |
| NH3(g) | -46,1 |
| CH4(g) | -74,8 |
| C2H5OH(l) | -277,7 |
Perhitungan Perubahan Entalpi Reaksi
Perubahan entalpi reaksi dapat dihitung dengan menggunakan data entalpi pembentukan standar. Rumusnya adalah:
ΔH°reaksi = ΣΔHf°(produk) – ΣΔHf°(reaktan)
Dimana:
* ΔH°reaksi adalah perubahan entalpi reaksi
* ΣΔHf°(produk) adalah jumlah entalpi pembentukan standar produk
* ΣΔHf°(reaktan) adalah jumlah entalpi pembentukan standar reaktan
Sebagai contoh, perhatikan reaksi pembakaran metana (CH4):
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
Perubahan entalpi reaksi dapat dihitung dengan menggunakan data entalpi pembentukan standar dari tabel di atas:
ΔH°reaksi = [ΔHf°(CO2(g)) + 2ΔHf°(H2O(l))] – [ΔHf°(CH4(g)) + 2ΔHf°(O2(g))]
ΔH°reaksi = [(-393,5 kJ/mol) + 2(-285,8 kJ/mol)] – [(-74,8 kJ/mol) + 2(0 kJ/mol)]
ΔH°reaksi = -890,3 kJ/mol
Hasil perhitungan menunjukkan bahwa perubahan entalpi reaksi pembakaran metana adalah -890,3 kJ/mol. Ini berarti bahwa reaksi pembakaran metana bersifat eksotermik, yaitu melepaskan energi sebesar 890,3 kJ per mol metana yang terbakar.
Entalpi Pembakaran Standar
Entalpi pembakaran standar adalah perubahan entalpi yang terjadi ketika satu mol zat dibakar sempurna dalam kondisi standar (suhu 298 K dan tekanan 1 atm). Reaksi pembakaran merupakan reaksi eksotermik, artinya melepaskan energi dalam bentuk panas ke lingkungan. Entalpi pembakaran standar dilambangkan dengan ΔH°c, dengan nilai negatif menunjukkan pelepasan panas.
Contoh Konkret Entalpi Pembakaran Standar
Sebagai contoh, pembakaran sempurna metana (CH4) menghasilkan karbon dioksida (CO2) dan air (H2O) dalam bentuk gas. Persamaan reaksi pembakaran metana adalah:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g)
Entalpi pembakaran standar metana adalah -890,3 kJ/mol. Nilai negatif ini menunjukkan bahwa reaksi pembakaran metana melepaskan 890,3 kJ energi panas per mol metana yang dibakar.
Tabel Entalpi Pembakaran Standar
Berikut adalah tabel yang berisi data entalpi pembakaran standar untuk berbagai senyawa:
| Senyawa | Rumus Kimia | ΔH°c (kJ/mol) |
|---|---|---|
| Metana | CH4 | -890,3 |
| Etanol | C2H5OH | -1367 |
| Propana | C3H8 | -2220 |
| Butana | C4H10 | -2877 |
| Glukosa | C6H12O6 | -2803 |
Contoh Perhitungan Perubahan Entalpi Reaksi
Misalnya, kita ingin menghitung perubahan entalpi reaksi untuk pembakaran 2 mol etanol. Dengan menggunakan data entalpi pembakaran standar etanol (-1367 kJ/mol), kita dapat menghitung perubahan entalpi reaksi sebagai berikut:
ΔH reaksi = 2 mol x (-1367 kJ/mol) = -2734 kJ
Hasil perhitungan menunjukkan bahwa pembakaran 2 mol etanol melepaskan 2734 kJ energi panas.
Soal Contoh 1
Perubahan entalpi reaksi dapat dihitung dengan menggunakan data entalpi pembentukan standar. Entalpi pembentukan standar adalah perubahan entalpi yang terjadi ketika satu mol senyawa dibentuk dari unsur-unsurnya dalam keadaan standar pada suhu 298 K dan tekanan 1 atm.
Contoh soal berikut akan menunjukkan bagaimana cara menghitung perubahan entalpi reaksi menggunakan data entalpi pembentukan standar.
Perhitungan Perubahan Entalpi Reaksi
Perhitungan perubahan entalpi reaksi menggunakan data entalpi pembentukan standar dilakukan dengan menggunakan rumus berikut:
ΔH° = ΣnΔH°f(produk) – ΣnΔH°f(reaktan)
Keterangan:
* ΔH° = perubahan entalpi reaksi standar
* ΔH°f = entalpi pembentukan standar
* n = koefisien stoikiometri
-
Contoh soal:
Hitunglah perubahan entalpi reaksi pembakaran metana (CH4) berdasarkan data entalpi pembentukan standar berikut:* ΔH°f CH4(g) = -74,8 kJ/mol
* ΔH°f CO2(g) = -393,5 kJ/mol
* ΔH°f H2O(l) = -285,8 kJ/mol -
Langkah pertama adalah menuliskan persamaan reaksi yang seimbang:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
-
Kemudian, hitung perubahan entalpi reaksi menggunakan rumus di atas:
ΔH° = [ΔH°f CO2(g) + 2ΔH°f H2O(l)] – [ΔH°f CH4(g) + 2ΔH°f O2(g)]
ΔH° = [(-393,5 kJ/mol) + 2(-285,8 kJ/mol)] – [(-74,8 kJ/mol) + 2(0 kJ/mol)]
ΔH° = -890,3 kJ/mol
- Jadi, perubahan entalpi reaksi pembakaran metana adalah -890,3 kJ/mol. Tanda negatif menunjukkan bahwa reaksi pembakaran metana adalah reaksi eksotermis, yaitu reaksi yang melepaskan kalor.
Contoh Soal 2: Penerapan Hukum Hess
Hukum Hess merupakan prinsip penting dalam kimia yang menyatakan bahwa perubahan entalpi reaksi tidak bergantung pada jalur reaksi, melainkan hanya bergantung pada keadaan awal dan akhir reaksi. Prinsip ini sangat berguna untuk menghitung perubahan entalpi reaksi yang sulit atau tidak mungkin dilakukan secara eksperimen. Berikut adalah contoh soal yang menunjukkan penerapan Hukum Hess:
Soal, Contoh soal perubahan entalpi reaksi dan pembahasannya
Tentukan perubahan entalpi standar (∆H°) untuk reaksi berikut:
C(s) + 2H2(g) → CH4(g)
Jika diketahui perubahan entalpi standar (∆H°) untuk reaksi berikut:
- C(s) + O2(g) → CO2(g) ; ∆H° = -393,5 kJ/mol
- H2(g) + 1/2O2(g) → H2O(l) ; ∆H° = -285,8 kJ/mol
- CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) ; ∆H° = -890,3 kJ/mol
Penyelesaian
Untuk menentukan perubahan entalpi standar (∆H°) reaksi yang ingin kita cari, kita perlu memanipulasi reaksi yang diketahui agar menghasilkan reaksi target. Berikut adalah langkah-langkahnya:
- Tulis kembali reaksi target: C(s) + 2H2(g) → CH4(g)
- Identifikasi reaksi yang diketahui yang mengandung reaktan dan produk target:
- Reaksi 1: C(s) + O2(g) → CO2(g)
- Reaksi 2: H2(g) + 1/2O2(g) → H2O(l)
- Reaksi 3: CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
- Manipulasi reaksi yang diketahui agar sesuai dengan reaksi target:
- Reaksi 1: C(s) + O2(g) → CO2(g) ; ∆H° = -393,5 kJ/mol (Tetap)
- Reaksi 2: 2[H2(g) + 1/2O2(g) → H2O(l)] ; ∆H° = 2(-285,8 kJ/mol) = -571,6 kJ/mol (Reaksi dikalikan 2)
- Reaksi 3: CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) ; ∆H° = -890,3 kJ/mol (Reaksi dibalik)
- Jumlahkan reaksi yang telah dimanipulasi:
- C(s) + O2(g) → CO2(g) ; ∆H° = -393,5 kJ/mol
- 2H2(g) + O2(g) → 2H2O(l) ; ∆H° = -571,6 kJ/mol
- CO2(g) + 2H2O(l) → CH4(g) + 2O2(g) ; ∆H° = +890,3 kJ/mol
Hasil penjumlahannya adalah:
C(s) + 2H2(g) → CH4(g)
- Hitung perubahan entalpi standar (∆H°) untuk reaksi target:
∆H° = ∆H°1 + ∆H°2 + ∆H°3 = -393,5 kJ/mol + (-571,6 kJ/mol) + 890,3 kJ/mol = -74,8 kJ/mol
Contoh soal perubahan entalpi reaksi dan pembahasannya memang sering muncul dalam pelajaran kimia. Misalnya, soal tentang perhitungan perubahan entalpi pembentukan suatu senyawa. Nah, untuk melatih kemampuan analisis dan pemahaman terhadap suatu topik, terkadang soal disajikan dalam bentuk essay.
Seperti contoh soal essay tentang artikel yang membahas tentang perubahan entalpi reaksi, kamu bisa temukan di situs ini. Dengan mengerjakan soal essay, kamu diajak untuk berpikir kritis dan mengelaborasi jawaban dengan lebih detail. Kembali ke soal perubahan entalpi reaksi, pemilihan metode perhitungan yang tepat dan pemahaman konsep hukum Hess akan membantumu menemukan jawaban yang akurat.
Kesimpulan
Berdasarkan perhitungan di atas, perubahan entalpi standar (∆H°) untuk reaksi pembentukan metana (CH4) dari karbon padat (C) dan gas hidrogen (H2) adalah -74,8 kJ/mol.
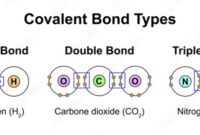
Contoh Soal 3: Perhitungan Entalpi Ikatan
Perhitungan perubahan entalpi reaksi menggunakan data entalpi ikatan merupakan metode yang efektif untuk menentukan perubahan energi yang terjadi selama reaksi kimia. Metode ini didasarkan pada konsep bahwa energi yang dibutuhkan untuk memutuskan ikatan kimia sama dengan energi yang dilepaskan saat ikatan tersebut terbentuk.
Perhitungan Entalpi Ikatan
Metode ini melibatkan penjumlahan entalpi ikatan yang putus pada reaktan dan pengurangannya dengan penjumlahan entalpi ikatan yang terbentuk pada produk. Rumus yang digunakan adalah:
ΔHreaksi = Σ (entalpi ikatan putus) – Σ (entalpi ikatan terbentuk)
Berikut adalah contoh soal perhitungan perubahan entalpi reaksi menggunakan data entalpi ikatan:
Contoh Soal
Hitunglah perubahan entalpi reaksi untuk reaksi pembakaran metana (CH4) berdasarkan data entalpi ikatan berikut:
| Ikatan | Entalpi Ikatan (kJ/mol) |
|—|—|
| C-H | 413 |
| O=O | 498 |
| C=O | 799 |
| O-H | 463 |
Reaksi pembakaran metana adalah:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g)
Penyelesaian
1. Identifikasi ikatan yang putus dan terbentuk:
– Ikatan yang putus: 4 ikatan C-H pada CH4 dan 2 ikatan O=O pada 2O2
– Ikatan yang terbentuk: 2 ikatan C=O pada CO2 dan 4 ikatan O-H pada 2H2O
2. Hitung jumlah entalpi ikatan yang putus:
– 4 (C-H) = 4 x 413 kJ/mol = 1652 kJ/mol
– 2 (O=O) = 2 x 498 kJ/mol = 996 kJ/mol
3. Hitung jumlah entalpi ikatan yang terbentuk:
– 2 (C=O) = 2 x 799 kJ/mol = 1598 kJ/mol
– 4 (O-H) = 4 x 463 kJ/mol = 1852 kJ/mol
4. Hitung perubahan entalpi reaksi:
– ΔHreaksi = Σ (entalpi ikatan putus) – Σ (entalpi ikatan terbentuk)
– ΔHreaksi = (1652 kJ/mol + 996 kJ/mol) – (1598 kJ/mol + 1852 kJ/mol)
– ΔHreaksi = -802 kJ/mol
Kesimpulan
Perubahan entalpi reaksi pembakaran metana adalah -802 kJ/mol. Nilai negatif menunjukkan bahwa reaksi ini melepaskan energi dan bersifat eksotermis.
Kesimpulan: Contoh Soal Perubahan Entalpi Reaksi Dan Pembahasannya
Memahami perubahan entalpi reaksi merupakan kunci untuk memahami dan memprediksi perubahan energi dalam reaksi kimia. Dengan mempelajari konsep ini, kita dapat memprediksi apakah suatu reaksi akan melepaskan atau menyerap panas, serta menghitung besarnya perubahan energi tersebut. Pengetahuan ini sangat berguna dalam berbagai bidang, seperti kimia, biologi, dan teknik, untuk mengembangkan teknologi dan proses yang lebih efisien dan ramah lingkungan.