Cara menghitung ph campuran – Menghitung pH campuran merupakan keterampilan penting dalam berbagai bidang, mulai dari kimia dan biologi hingga industri dan lingkungan. Memahami bagaimana pH berubah ketika dua atau lebih larutan dicampur dapat membantu kita dalam mengendalikan reaksi kimia, menganalisis sampel, dan menjaga keseimbangan lingkungan.
Bayangkan Anda sedang membuat minuman jus jeruk. Anda ingin memastikan rasa asamnya pas, tidak terlalu asam atau terlalu manis. Dalam kasus ini, menghitung pH campuran jus jeruk dapat membantu Anda menentukan berapa banyak air atau gula yang harus ditambahkan untuk mencapai rasa yang tepat. Artikel ini akan memandu Anda melalui konsep pH campuran, faktor-faktor yang mempengaruhinya, dan metode praktis untuk menghitungnya.
Pengertian pH Campuran: Cara Menghitung Ph Campuran

Dalam dunia kimia, pH merupakan skala yang digunakan untuk mengukur tingkat keasaman atau kebasaan suatu larutan. pH campuran, sebagaimana namanya, merujuk pada pH yang dihasilkan ketika dua atau lebih larutan dengan pH berbeda dicampur. Pencampuran ini dapat menghasilkan larutan dengan pH yang lebih asam, lebih basa, atau bahkan netral, tergantung pada sifat kimia dan konsentrasi masing-masing larutan.
Contoh pH Campuran dalam Kehidupan Sehari-hari
Contoh sederhana pH campuran dapat kita temui dalam kehidupan sehari-hari. Misalnya, saat kita menambahkan cuka (asam) ke dalam larutan baking soda (basa), terjadi reaksi kimia yang menghasilkan gelembung karbon dioksida dan perubahan pH. Atau, ketika kita mencampur air jeruk nipis (asam) dengan air gula (netral), pH campuran akan menjadi lebih asam.
Perbedaan pH antara Larutan Asam, Basa, dan Netral
| Jenis Larutan | pH | Contoh |
|---|---|---|
| Asam | Kurang dari 7 | Cuka, air jeruk nipis, asam lambung |
| Basa | Lebih dari 7 | Sabun, soda kue, air sabun |
| Netral | 7 | Air murni |
Faktor yang Mempengaruhi pH Campuran
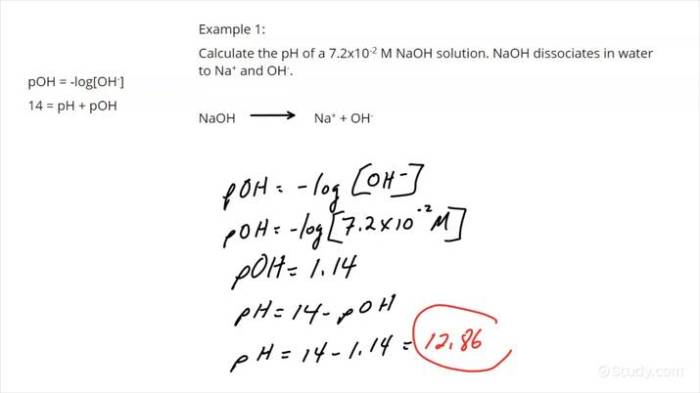
Ketika mencampur dua atau lebih larutan, pH campuran yang dihasilkan tidak selalu menjadi rata-rata dari pH larutan awal. Ada beberapa faktor yang dapat mempengaruhi pH campuran, yang perlu dipahami untuk memprediksi dan mengendalikan pH akhir.
Konsentrasi Asam dan Basa
Konsentrasi asam dan basa dalam larutan merupakan faktor utama yang menentukan pH campuran. Semakin tinggi konsentrasi asam, semakin rendah pH-nya, dan sebaliknya. Begitu pula dengan basa, semakin tinggi konsentrasinya, semakin tinggi pH-nya. Ketika mencampur asam dan basa, konsentrasi relatif dari masing-masing komponen menentukan pH akhir.
Pengaruh Suhu
Suhu juga dapat mempengaruhi pH campuran, meskipun pengaruhnya tidak selalu signifikan. Pada umumnya, peningkatan suhu akan menyebabkan penurunan pH untuk larutan asam dan peningkatan pH untuk larutan basa. Hal ini dikarenakan suhu mempengaruhi kesetimbangan ionisasi asam dan basa, yang pada gilirannya mempengaruhi konsentrasi ion hidrogen (H+) dan hidroksida (OH-) dalam larutan. Sebagai contoh, air murni memiliki pH 7 pada suhu kamar, tetapi pada suhu 100°C, pH-nya akan turun menjadi sekitar 6,14.
Metode Menghitung pH Campuran
Menghitung pH campuran dapat menjadi proses yang rumit, terutama ketika melibatkan asam dan basa dengan konsentrasi berbeda. Namun, dengan menggunakan metode yang tepat, kita dapat menentukan pH campuran dengan akurasi yang cukup tinggi. Salah satu metode yang paling umum digunakan adalah metode Henderson-Hasselbalch.
Rumus Henderson-Hasselbalch
Rumus Henderson-Hasselbalch merupakan persamaan yang berguna untuk menghitung pH larutan penyangga, yaitu larutan yang terdiri dari asam lemah dan basa konjugatnya atau basa lemah dan asam konjugatnya. Rumus ini membantu kita menentukan pH campuran berdasarkan konsentrasi asam dan basa dalam campuran tersebut.
pH = pKa + log ([basa]/[asam])
Dimana:
- pH adalah potensial hidrogen, yang menunjukkan tingkat keasaman atau kebasaan suatu larutan.
- pKa adalah negatif logaritma dari konstanta disosiasi asam (Ka), yang merupakan ukuran kekuatan asam.
- [basa] adalah konsentrasi basa konjugat dalam larutan.
- [asam] adalah konsentrasi asam lemah dalam larutan.
Contoh Perhitungan pH Campuran, Cara menghitung ph campuran
Misalkan kita memiliki larutan penyangga yang terdiri dari 0,1 M asam asetat (CH3COOH) dan 0,2 M natrium asetat (CH3COONa). Asam asetat adalah asam lemah dengan pKa = 4,76. Untuk menghitung pH campuran, kita dapat menggunakan rumus Henderson-Hasselbalch:
pH = 4,76 + log (0,2/0,1)
pH = 4,76 + log (2)
pH = 4,76 + 0,301
pH = 5,06
Jadi, pH campuran larutan penyangga tersebut adalah 5,06. Ini menunjukkan bahwa larutan tersebut bersifat sedikit asam.
Tabel dan Diagram
Tabel dan diagram dapat membantu kita dalam memvisualisasikan dan memahami perhitungan pH campuran. Berikut adalah contoh tabel dan diagram yang dapat digunakan:
| Asam Lemah | Basa Konjugat | pKa | pH |
|---|---|---|---|
| Asam Asetat (CH3COOH) | Natrium Asetat (CH3COONa) | 4,76 | 5,06 |
Diagram berikut menunjukkan hubungan antara pH dan konsentrasi asam dan basa dalam larutan penyangga. Garis horizontal menunjukkan pH larutan, sedangkan garis vertikal menunjukkan konsentrasi asam dan basa.
Diagram ini menunjukkan bahwa pH larutan penyangga berada di sekitar pKa asam lemah. Ketika konsentrasi asam dan basa sama, pH larutan sama dengan pKa. Ketika konsentrasi basa lebih tinggi daripada asam, pH larutan akan lebih tinggi dari pKa. Sebaliknya, ketika konsentrasi asam lebih tinggi daripada basa, pH larutan akan lebih rendah dari pKa.
Penutupan Akhir

Dengan memahami konsep pH campuran, kita dapat lebih akurat dalam mengendalikan reaksi kimia, menganalisis sampel, dan bahkan menjaga keseimbangan lingkungan. Pengetahuan ini membuka peluang untuk penelitian, inovasi, dan solusi yang lebih baik untuk berbagai masalah.